Introducere
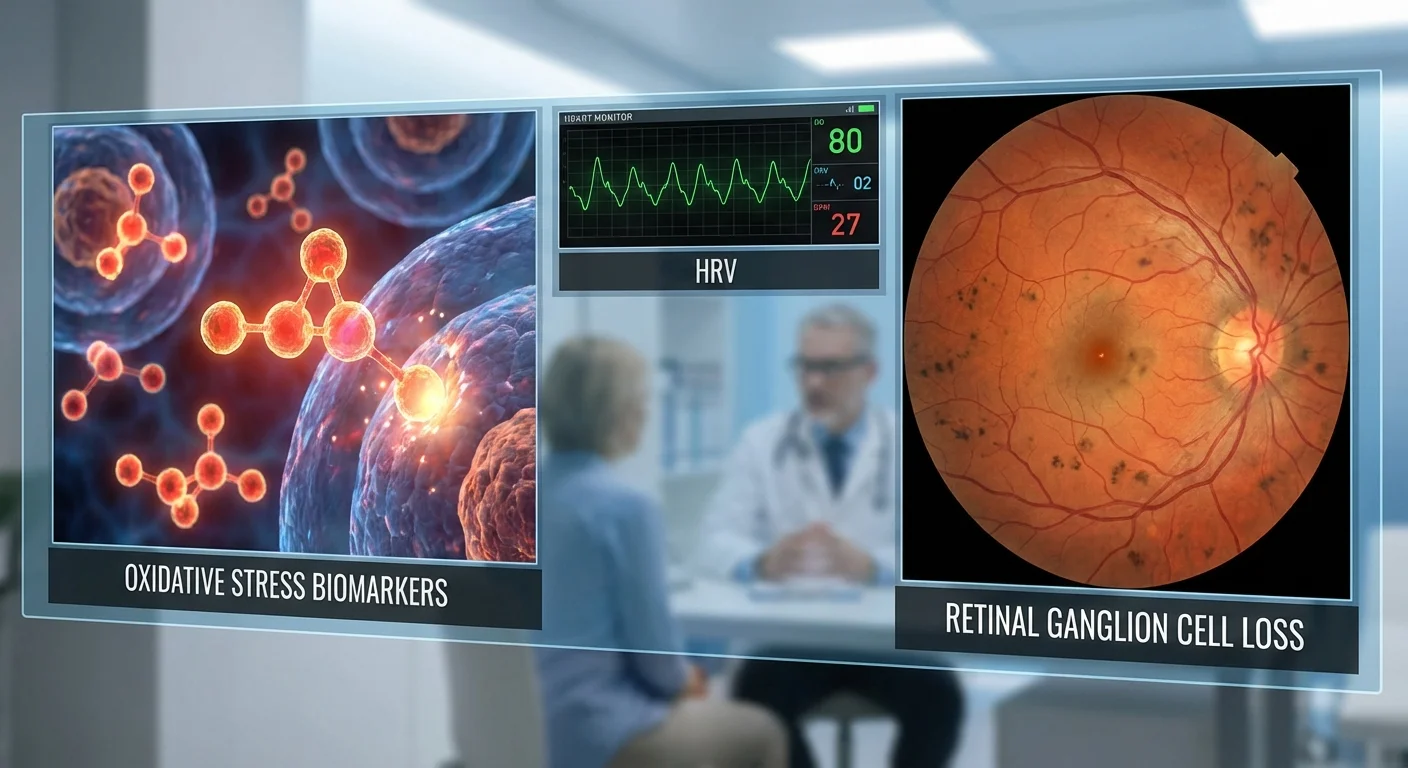
Glaucomul este o boală oculară în care celulele ganglionare retiniene (CGR) – celulele nervoase care transmit semnale vizuale de la ochi la creier – mor lent. Acest lucru provoacă o pierdere graduală, ireversibilă a vederii. Medicii se concentrează de obicei pe scăderea presiunii intraoculare pentru a încetini progresia glaucomului, dar cercetările arată acum că stresul oxidativ (un tip de stres chimic în corp) și dezechilibrele din sistemul nervos autonom (sistemul nervos „automat” care controlează funcții precum ritmul cardiac) joacă, de asemenea, un rol. La pacienții cu glaucom, nivelurile sanguine ale anumitor markeri redox – substanțe care indică daune oxidative – tind să fie mai mari decât în mod normal. În același timp, mulți pacienți cu glaucom prezintă variabilitate redusă a ritmului cardiac (VRC), un semn de dezechilibru autonom. Împreună, stresul oxidativ crescut și reglarea autonomă deficitară pot agrava leziunile CGR.
În acest articol, explicăm ce sunt markerii de stres oxidativ precum F2-izoprostane, malondialdehida (MDA) și 8-hidroxi-2'-deoxiguanozina (8-OHdG) și cum sunt găsiți în glaucom. Definim VRC (variabilitatea ritmului cardiac) și examinăm cum este aceasta modificată în glaucom. Descriem posibilele căi biologice care leagă stresul oxidativ și dezechilibrul autonom de o moarte mai rapidă a CGR. Apoi, rezumăm ce au arătat studiile despre antioxidanți (nutrienți care combat stresul oxidativ) asupra rezultatelor glaucomului. În final, sugerăm viitoare studii „multi-omice” care combină markerii redox din sânge sau urină, măsurători ale VRC și imagistică retiniană avansată pentru noi perspective.
Pe parcurs, ne concentrăm pe informații pe care pacienții le pot înțelege și pe baza cărora pot acționa. Explicăm, de asemenea, ce teste de stres oxidativ pot fi comandate (prin sânge sau urină) și ce ar putea însemna citirile ridicate sau scăzute pentru o persoană preocupată de glaucom.
Markerii de Stres Oxidativ în Glaucom
Stresul oxidativ înseamnă că există prea mulți „radicali liberi” (molecule reactive de oxigen) în corp, provocând daune celulelor. Nu putem măsura direct radicalii liberi cu ușurință, așa că medicii și cercetătorii folosesc biomarkeri în sânge sau urină care indică leziuni oxidative. Trei markeri importanți în glaucom sunt F2-izoprostane, malondialdehida (MDA) și 8-hidroxi-2'-deoxiguanozina (8-OHdG). Toți trei cresc atunci când stresul oxidativ se intensifică.
-
F2-Izoprostane (8-iso-PGF2α) – acestea sunt molecule stabile formate atunci când grăsimile (grăsimile polinesaturate din membranele celulare) oxidează. F2-izoprostanele sunt considerate un „standard de aur” pentru măsurarea oxidării lipidelor (grăsimilor) (pmc.ncbi.nlm.nih.gov). Nivelurile sanguine sau urinare mai ridicate ale acestora sugerează că celulele sunt sub atac oxidativ. Deși nu toate studiile despre glaucom le măsoară, niveluri ridicate de F2-izoprostane au fost găsite în multe boli și se crede că reflectă un stres oxidativ puternic (pmc.ncbi.nlm.nih.gov). (În practică, laboratoarele pot măsura F2-izoprostanele în urină sau plasmă folosind echipamente specializate, dar acest lucru se face mai ales în cadrul cercetărilor.)
-
Malondialdehida (MDA) – această substanță chimică este produsă atunci când speciile reactive de oxigen descompun grăsimile în corp. La fel ca F2-izoprostanele, semnalează deteriorarea grăsimilor prin oxidare. Multiple studii despre glaucom au constatat că pacienții cu glaucom au MDA mai mare în sânge decât persoanele sănătoase (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). De fapt, o revizuire amplă a constatat că MDA a fost cel mai constant marker de stres oxidativ ridicat în sângele pacienților cu glaucom (pmc.ncbi.nlm.nih.gov). Într-un studiu privind glaucomul cu unghi închis, pacienții au avut MDA semnificativ mai mare decât subiecții de control (pmc.ncbi.nlm.nih.gov). În mod remarcabil, acel studiu a arătat că pacienții cu niveluri foarte ridicate de MDA au avut o pierdere mai rapidă a vederii: cei cu MDA peste aproximativ 12 unități au avut un declin mult mai rapid al câmpului vizual (pmc.ncbi.nlm.nih.gov).
-
8-Hidroxi-2'-deoxiguanozină (8-OHdG) – acest marker indică leziuni oxidative ale ADN-ului (materialul genetic din celule). Atunci când stresul oxidativ taie sau modifică ADN-ul, nivelurile de 8-OHdG cresc și pot fi măsurate în sânge sau urină. Studiile pe pacienții cu glaucom (în glaucom cu tensiune normală și pseudoexfoliativ) au găsit niveluri semnificativ mai mari de 8-OHdG în plasmă decât la subiecții de control (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). De exemplu, un studiu a constatat că 8-OHdG mediu în sânge era de aproximativ 17 ng/mL la persoanele sănătoase și de ~23 ng/mL la pacienții cu glaucom (pmc.ncbi.nlm.nih.gov). Un alt raport a arătat că riscul de glaucom era de peste 4 ori mai mare la persoanele al căror 8-OHdG era peste un anumit prag (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Pe scurt, 8-OHdG ridicat înseamnă mai multe leziuni ale ADN-ului de la oxigenul reactiv, iar acest lucru este observat la pacienții cu glaucom.
Alți markeri măsurați ocazional includ nivelurile totale de antioxidanți (cum ar fi „starea antioxidantă totală” sau enzime precum superoxid dismutaza (SOD) și glutation peroxidaza). În multe studii despre glaucom, acești antioxidanți sunt scăzuți (deoarece au fost consumați luptând împotriva radicalilor liberi), în timp ce markeri precum MDA, 8-OHdG sau H₂O₂ sunt ridicați (pmc.ncbi.nlm.nih.gov). (Pentru concizie, ne concentrăm aici pe F2-izoprostane, MDA și 8-OHdG, dar multe studii raportează enzime antioxidante și vitamine mai scăzute în glaucom.)
Rezumat: La pacienții cu glaucom, studiile observă în mod constant daune oxidative mai mari în corp. Markeri precum MDA și 8-OHdG tind să fie peste intervalul normal observat la persoanele sănătoase (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Cercetătorii cred că acest stres oxidativ suplimentar contribuie la efectele glaucomului asupra nervului optic.
Măsurarea Stresului Oxidativ: Teste Disponibile
Deși acești markeri sunt importanți în cercetare, ei nu sunt încă teste clinice de rutină. Cu toate acestea, unele laboratoare specializate și clinici de sănătate oferă panouri de stres oxidativ. Iată ce ar trebui să știe pacienții:
-
Testul 8-OHdG: Poate fi măsurat în plasma sanguină sau în urină. Există kituri comerciale (teste ELISA) pentru a măsura 8-OHdG în urină (de exemplu, kitul Genox „8-OHdG Check” (www.genox.com)). Un furnizor de servicii medicale poate aranja acest lucru prin laboratoare specializate. Nu există un nivel „normal” universal, dar studiile oferă o idee. De exemplu, un studiu despre glaucom a constatat că pacienții de control aveau o medie de ~17 ng/mL, în timp ce pacienții cu glaucom aveau o medie de ~23 ng/mL (pmc.ncbi.nlm.nih.gov). Dacă 8-OHdG-ul dumneavoastră este mult mai mare decât valorile tipice sănătoase, sugerează leziuni crescute ale ADN-ului cauzate de stresul oxidativ.
-
Testul F2-izoprostane: De obicei măsurat într-o probă de urină de 24 de ore sau, uneori, în sânge. Este considerat foarte fiabil, dar necesită echipament de laborator (spectrometrie de masă). Valorile normale depind de vârstă și metodă, dar din nou, un rezultat mult mai mare sugerează o peroxidare lipidică crescută. Acest test se efectuează în principal în cercetare sau în centre specializate.
-
Testul MDA: Malondialdehida poate fi măsurată în plasma sanguină (adesea prin metoda „substanțelor reactive cu acidul tiobarbituric” sau TBARS, sau prin cromatografie). Intervalele normale de laborator variază, dar un studiu despre glaucom a folosit un prag de ~12 µmol/L pentru a semnala un risc mai mare (pmc.ncbi.nlm.nih.gov). Dacă raportul de laborator arată MDA ridicat peste valorile tipice (întrebați intervalul de referință al laboratorului), acest lucru poate indica un stres oxidativ excesiv asupra grăsimilor.
-
Teste pentru Antioxidanți Totali sau Enzime: Unele laboratoare măsoară „capacitatea antioxidantă totală” sau nivelurile de SOD sau glutation peroxidază. Rezultatele sub normal indică din nou stres oxidativ, deoarece antioxidanții sunt consumați.
În practică, aceste teste nu sunt standard precum colesterolul sau glicemia. Dacă doriți să fie verificate, ar putea fi necesar să solicitați un laborator specializat sau să consultați un medic care le poate comanda. Rețineți că rezultatele trebuie interpretate în context de către un profesionist. Factori precum dieta, ora din zi sau exercițiile fizice pot afecta acești markeri.
După cum subliniază o revizuire, stresul oxidativ nu este evaluat în mod obișnuit în practica zilnică (pmc.ncbi.nlm.nih.gov), deoarece speciile reactive de oxigen în sine au o durată de viață scurtă. În schimb, medicii se uită la markeri indirecți (cum cei de mai sus) sau se concentrează pe reducerea stresului prin stilul de viață. Dacă obțineți rezultate ale testelor, comparați-le cu orice „interval normal” furnizat și discutați cu medicul dumneavoastră. În general, 8-OHdG, MDA sau izoprostanele mai mari decât normalul indică un stres oxidativ crescut, în timp ce nivelurile în intervalul normal sunt liniștitoare.
Funcția Autonomă și Variabilitatea Ritmului Cardiac în Glaucom
Sistemul nervos autonom (SNA) controlează funcțiile involuntare precum ritmul cardiac, tonusul vaselor de sânge și digestia. Are două ramuri – simpatică (adesea numită „luptă sau fugi”) și parasimpatică (odihnă/digestie). Un echilibru sănătos între ele determină un ritm cardiac care variază constant. Variabilitatea ritmului cardiac (VRC) este o măsură a cât de mult fluctuează timpul dintre bătăile inimii. În termeni simpli, o VRC mai mare înseamnă că inima răspunde flexibil (adesea un semn de sănătate bună), în timp ce o VRC foarte scăzută sugerează dezechilibru autonom, de obicei prea multă activitate simpatică sau un ton parasimpatic redus.
Studii recente arată că pacienții cu glaucom au adesea VRC redusă comparativ cu persoanele fără glaucom (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). De exemplu, într-un studiu amplu, pacienții cu glaucom exfoliativ (o formă de glaucom cu unghi deschis) au avut metrici VRC semnificativ mai scăzute decât controalele sănătoase (pmc.ncbi.nlm.nih.gov). O altă analiză a constatat că pacienții cu glaucom cu cea mai scăzută VRC (dominanță simpatică cea mai puternică) au avut o subțiere mult mai rapidă a stratului nervos optic din retină decât cei cu VRC mai mare (pmc.ncbi.nlm.nih.gov). În acel studiu, grupul cu VRC scăzută a pierdut aproximativ 1,4 μm din grosimea fibrei nervoase pe an (față de doar 0,3 μm/an în grupul cu VRC ridicată) (pmc.ncbi.nlm.nih.gov). Au avut, de asemenea, mai multe fluctuații ale presiunii intraoculare și o presiune de perfuzie oculară mai scăzută, indicând că dezechilibrul autonom afectează fluxul sanguin ocular.
Pe scurt, glaucomul – în special anumite tipuri precum glaucomul exfoliativ – tinde să fie însoțit de disfuncție SNA. Studiile observă în mod constant că pacienții cu glaucom au variații mai mici ale ritmului cardiac decât persoanele sănătoase (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). O VRC mai scăzută este un semnal de stres cronic sau de nervi simpatici hiperactivi. Important este că VRC scăzută în glaucom a fost legată de rezultate mai slabe: pacienții cu VRC diminuată au avut o pierdere mai rapidă a fibrelor nervoase retiniene și mai multe defecte ale vederii centrale (pmc.ncbi.nlm.nih.gov).
Măsurarea VRC: O persoană poate măsura VRC cu dispozitive precum monitoare cardiace sau chiar unele ceasuri inteligente și smartphone-uri care utilizează senzori de puls. Clinicile utilizează uneori un EKG scurt sau un analizor portabil VRC (cum ar fi un senzor de deget). Dacă VRC-ul dumneavoastră este mai scăzut decât media pentru vârsta și sexul dumneavoastră, sugerează stres autonom. De exemplu, studiul [26] a folosit SDNN (o măsură standard a VRC) pentru a împărți pacienții în grupuri cu VRC „scăzută” vs „ridicată”. Deși nu există praguri simple publicate, un SDNN sub aproximativ 50 ms este adesea considerat scăzut la adulți. Cu toate acestea, consultați medicul dumneavoastră cu datele VRC brute; acesta le poate utiliza împreună cu alte informații de sănătate, mai degrabă decât singure.
Conexiunea cu Stresul Oxidativ: O VRC scăzută înseamnă că organismul se află într-o stare de stres mai ridicată. În multe afecțiuni (cum ar fi boala renală cronică sau bolile de inimă), cercetătorii au constatat că biomarkerii de stres oxidativ mai ridicați merg mână în mână cu o VRC mai scăzută (pmc.ncbi.nlm.nih.gov). Într-un studiu pe pacienți cu boală renală, cei cu niveluri ridicate de F2-izoprostane în plasmă (o măsură a stresului oxidativ) au avut o VRC semnificativ redusă (pmc.ncbi.nlm.nih.gov). Deși această legătură exactă nu a fost studiată extensiv în glaucom, ea sugerează un ciclu: stresul oxidativ poate afecta vasele de sânge și nervii, ducând la dezechilibru autonom, care la rândul său poate agrava fluxul sanguin și stresul asupra ochilor.
Cum Stresul Oxidativ și Dezechilibrul Autonom Pot Accelera Pierderea CGR
Pentru a înțelege cum stresul oxidativ și dezechilibrul SNA ar putea determina moartea mai rapidă a celulelor ganglionare retiniene (CGR), luați în considerare aceste căi interconectate:
-
Leziuni oxidative directe ale CGR: CGR sunt neuroni cu cerințe energetice foarte ridicate (în special axonii lor lungi, nemielinizați, din interiorul retinei) (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Ele se bazează puternic pe mitocondrii (centralele energetice ale celulei) pentru a produce ATP. Mitocondriile eliberează în mod natural specii reactive de oxigen (SRO) în timpul producției de energie. Dacă producția de SRO este prea mare sau apărarea antioxidantă a celulei este slabă, SRO în exces se acumulează. În CGR, aceasta înseamnă leziuni oxidative ale ADN-ului, proteinelor și lipidelor. De exemplu, 8-OHdG se formează atunci când SRO deteriorează ADN-ul din CGR. Odată ce ADN-ul și membranele mitocondriale sunt deteriorate, procesele celulare cheie eșuează. Nivelurile cronic ridicate de SRO declanșează programul de moarte celulară încorporat (apoptoza) prin eliberarea de factori precum citocromul c din mitocondrii (pmc.ncbi.nlm.nih.gov). În termeni simpli, prea mult stres oxidativ otrăvește CGR și le face să se autodistrugă. Acest lucru a fost observat în multe studii oculare: SRO în exces au fost găsite în celulele retiniene după leziuni, iar adăugarea de antioxidanți poate bloca daunele în modele animale (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov).
-
Efecte vasculare (flux sanguin): Dezechilibrul autonom (supraactivitate simpatică) poate îngusta vasele de sânge și reduce fluxul sanguin către ochi. În glaucom, aportul sanguin adecvat este critic pentru supraviețuirea CGR. De exemplu, studiul [26] a arătat că pacienții cu VRC scăzută au avut o presiune de perfuzie oculară mai scăzută (presiunea arterială efectivă care irigă nervul optic) și mai multe fluctuații de la an la an ale presiunii intraoculare. Tensiunea arterială scăzută sau creșterea bruscă a presiunii intraoculare pot priva intermitent CGR de oxigen. Ischemia (lipsa de oxigen) în sine provoacă stres oxidativ – atunci când aportul de oxigen revine, generează SRO (leziuni de ischemie-reperfuzie). Astfel, vasoconstricția și instabilitatea fluxului sanguin determinate de SNA creează un ciclu de hipoxie și leziuni oxidative ale CGR (pmc.ncbi.nlm.nih.gov).
-
Inflamație și stres celular: Stresul oxidativ poate inflama celulele de susținere din retină (celulele gliale). Aceste celule eliberează apoi molecule inflamatorii care stresează și mai mult CGR. Între timp, disfuncția autonomă este adesea legată de inflamația sistemică de grad scăzut. Împreună, SRO excesive și o stare simpatizată ar putea amplifica inflamația dăunătoare în jurul capului nervului optic, accelerând moartea CGR.
-
Interacțiuni cu stresul mecanic: Presiunea intraoculară (PIO) ridicată deformează capul nervului optic, întinzând axonii CGR. Axonii stresați devin înfometați de energie și produc mai multe SRO. Dacă antioxidanții sunt scăzuți (așa cum se observă la pacienții cu glaucom), SRO suplimentare înclină balanța spre moartea celulară. Dezechilibrul SNA poate agrava fluctuațiile PIO și reduce capacitatea ochiului de a regla PIO și fluxul sanguin, amplificând acest efect (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov).
Pe scurt, stresul oxidativ dăunează CGR la nivel celular, în timp ce problemele autonome/vasculare autonome afectează aportul sanguin și vindecarea CGR. O revizuire majoră a glaucomului a spus concis: apoptoza CGR în glaucom este determinată de PIO crescută, flux sanguin slab („insuficiență vasculară”) și stres oxidativ (pmc.ncbi.nlm.nih.gov). Acești factori acționează împreună: stresul oxidativ lezează mitocondriile și ADN-ul CGR (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov), în timp ce stresul autonom provoacă ischemie retiniană și lipsă de nutrienți, ducând la apoptoza CGR mai rapidă. La pacienți, acest lucru se manifestă ca o pierdere mai rapidă a fibrelor nervului optic și a vederii atunci când VRC este scăzută (pmc.ncbi.nlm.nih.gov) sau markerii oxidativi sunt ridicați (pmc.ncbi.nlm.nih.gov).
Intervenții Antioxidante și Rezultatele Glaucomului
Deoarece glaucomul implică leziuni oxidative, multe studii s-au întrebat dacă suplimentele antioxidante pot ajuta la protejarea ochiului. Antioxidanții includ vitamine (C, E), nutrienți precum coenzima Q10, flavonoide (din fructe/ceai), acizi grași omega-3 și extracte din plante (precum Gingko biloba). Aceste substanțe pot neutraliza radicalii liberi, cel puțin în teorie.
Constatări de laborator și animale: În modele animale de glaucom sau leziuni oculare, administrarea de antioxidanți a redus adesea pierderea CGR. De exemplu, la șobolani cu glaucom sau ischemie retiniană, suplimente precum vitamina A, Ginkgo, acid alfa-lipoic, coenzima Q10, acizi grași omega-3 și resveratrol au arătat toate o anumită protecție a celulelor retiniene (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Un tabel dintr-o revizuire listează multe experimente: de exemplu, extractul de Ginkgo biloba a redus moartea CGR la ochii de șobolan cu presiune ridicată (pmc.ncbi.nlm.nih.gov); coenzima Q10 și vitamina E au protejat celulele retiniene cultivate de toxinele oxidative (pmc.ncbi.nlm.nih.gov); iar antioxidanții alimentari (cum ar fi antocianinele din fructe) au ajutat la păstrarea structurii retiniene în modele animale de glaucom (pmc.ncbi.nlm.nih.gov). Aceste studii sugerează că antioxidanții pot ajuta celulele retiniene să supraviețuiască stresului.
Studii clinice umane: Studiile la pacienții cu glaucom au fost mai mici și mixte, dar unele sunt încurajatoare. O revizuire sistematică recentă a 15 studii randomizate a constatat că suplimentele antioxidante au îmbunătățit semnificativ rezultatele legate de glaucom (pmc.ncbi.nlm.nih.gov). În medie, pacienții care au luat antioxidanți (vitamine, coenzima Q10, luteină etc.) au avut o presiune intraoculară mai mică, o pierdere mai lentă a câmpului vizual și un flux sanguin ocular mai bun decât cei care au luat placebo (pmc.ncbi.nlm.nih.gov). Important este că nu au existat mai multe efecte secundare (cum ar fi modificări ale tensiunii arteriale) în grupul cu antioxidanți decât în cel cu placebo, deci au părut sigure (pmc.ncbi.nlm.nih.gov).
Unele constatări umane specifice: într-un studiu din 2003, pacienții cu glaucom care au luat extract de Ginkgo biloba au avut îmbunătățiri modeste ale indicilor câmpului vizual (pmc.ncbi.nlm.nih.gov). Un studiu ulterior a confirmat că pacienții cu NVG (glaucom cu tensiune normală) care au luat Ginkgo au avut un flux sanguin mai bun în jurul nervului optic (pmc.ncbi.nlm.nih.gov). Alte studii mici au găsit beneficii pentru extractul de ceai verde (epigallocatechin gallate) asupra funcției retiniene, sau antocianinele de coacăz negru care stimulează circulația oculară (deși PIO sau vederea nu s-au modificat mult) (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). O combinație de extracte botanice (forskolin+rutină) chiar a redus PIO cu aproximativ 10% în plus față de picăturile obișnuite (pmc.ncbi.nlm.nih.gov).
Cu toate acestea, este corect să spunem că rezultatele sunt variabile. Unele studii cu antioxidanți arată câștiguri modeste sau deloc. Diferențele de doză, tip de pacient și mărime a studiului contează. În general, majoritatea dovezilor sugerează că adăugarea de antioxidanți este promițătoare și sigură, dar nu este încă un remediu de sine stătător. Revizuirile majore concluzionează că ar putea ajuta la încetinirea deteriorării glaucomatoase (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov), dar sunt încă necesare studii definitive mai mari.
Concluzie practică: Cel puțin, o dietă sănătoasă bogată în antioxidanți (fructe, legume cu frunze verzi, omega-3) pare înțeleaptă pentru sănătatea ochilor. Unii oftalmologi recomandă deja suplimente precum vitaminele C/E, luteina sau omega-3 pacienților cu glaucom ca o măsură suplimentară. Verificați cu medicul dumneavoastră înainte de a începe orice pastile, mai ales în doze mari. Cercetările de până acum implică faptul că astfel de suplimente nu vor dăuna și ar putea ajuta aspecte ale glaucomului precum fluxul sanguin sau sănătatea nervilor (pmc.ncbi.nlm.nih.gov).
Direcții Viitoare: Integrarea Redox, VRC și Imagistică Retiniană
Cercetătorii prevăd acum studii mai integratoare – așa-numitele multi-omics – pentru a învinge glaucomul. Aceasta înseamnă colectarea multor tipuri de date împreună: markeri din sânge (sau urină) ai echilibrului redox, înregistrări continue ale VRC, imagini retiniene detaliate și chiar profiluri genetice sau metabolice. Punând toate piesele împreună, s-ar putea găsi tipare invizibile în izolare.
De exemplu, metabolomica modernă (măsurarea a zeci de molecule mici în sânge) a dezvăluit deja semnături unice în glaucom. O revizuire a studiilor metabolomice umane a constatat niveluri alterate de aminoacizi, lipide și căi conexe la pacienții cu glaucom (pmc.ncbi.nlm.nih.gov). Aceste modificări metabolice sugerează procese subiacente care ar putea fi țintite. Combinând acest lucru cu datele VRC (interacțiuni intestin-creier-SNA) și imagistica OCT de înaltă rezoluție a nervului optic și a straturilor retiniene, cercetătorii ar putea clasifica pacienții în subgrupuri. Poate că unii pacienți au un profil „cu stres oxidativ ridicat” (8-OHdG foarte ridicat, VRC scăzută și stratul fibrei nervoase retiniene mai subțire la OCT), în timp ce alții nu.
O paralelă poate fi observată în cercetările privind retinopatia diabetică: un studiu recent la șoareci a utilizat o abordare multi-omică, combinând transcriptomica țesutului retinian, metabolomica serului sanguin și datele genetice (GWAS), pentru a lega modificările metabolice sanguine cu inflamația retiniană timpurie (pmc.ncbi.nlm.nih.gov). Aplicarea unei strategii similare la glaucom – de exemplu, legarea metabolismului periferic de pierderea fibrelor nervoase retiniene – ar putea descoperi noi ținte medicamentoase sau markeri de screening. De exemplu, dacă anumiți metaboliți sanguini cresc în mod constant înainte de orice pierdere a vederii, aceștia ar putea deveni biomarkeri de avertizare timpurie.
Ce înseamnă acest lucru pentru pacienți: În viitor, o vizită la medic ar putea implica un panel de analize simple de sânge (sau urină) pentru mai mulți markeri de stres oxidativ, o măsurare a VRC (cum ar fi un EKG de cinci minute sau un monitor portabil acasă) și imagistică oculară avansată. Analizarea tuturor rezultatelor împreună ar putea prezice cine prezintă cel mai mare risc de progresie. Mai mult, dacă se constată că un biomarker specific (să zicem, F2-izoprostane foarte ridicate) este responsabil de daune, s-ar putea adapta tratamentul pentru a reduce acel stres sau pentru a utiliza antioxidanți țintiți.
Deocamdată, nu am ajuns încă acolo, dar cercetarea multi-omică a glaucomului este o direcție promițătoare. Speranța este de a depăși concentrarea exclusivă pe presiunea intraoculară și de a construi o imagine mai completă a bolii fiecărui pacient.
Concluzie
Glaucomul este mai mult decât o presiune intraoculară ridicată – este legat de stresul oxidativ generalizat în corp și de disfuncția sistemului nervos autonom. Pacienții cu glaucom tind să aibă niveluri mai ridicate de markeri sanguini precum MDA și 8-OHdG, indicând deteriorarea celulelor și a ADN-ului (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). În același timp, aceștia prezintă adesea variabilitate redusă a ritmului cardiac, reflectând o supraactivitate simpatică (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Acești doi factori acționează probabil împreună pentru a distruge celulele ganglionare retiniene mai rapid. Stresul oxidativ deteriorează mitocondriile și ADN-ul CGR (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov), în timp ce dezechilibrul autonom duce la un flux sanguin ocular slab și la fluctuații ale presiunii (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov).
Există dovezi solide că antioxidanții pot ajuta – studiile pe animale arată în mod constant protecția CGR (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov), iar studiile pe oameni indică faptul că suplimentele pot îmbunătăți câmpul vizual și fluxul sanguin ocular (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Pacienții pot discuta cu oftalmologul lor despre vitamine și nutrienți antioxidanți ca parte a unei abordări de stil de viață sănătos.
Important este că unele teste de stres oxidativ (8-OHdG, MDA, izoprostane din sânge sau urină) sunt accesibile, deși nu de rutină. Dacă acestea sunt măsurate, valorile ridicate (cum ar fi 8-OHdG mult peste ~20 ng/mL sau MDA peste intervalele cunoscute de laborator) ar trebui să determine atenție sporită la dietă, stil de viață și, posibil, suport antioxidant. Similar, măsurarea VRC (cu un simplu monitor de acasă sau EKG la clinică) poate indica sănătatea autonomă; o VRC scăzută poate însemna stres suplimentar asupra ochilor.
În viitor, combinarea acestor măsuri cu imagistica retiniană avansată și datele genetice în studii integrative poate oferi o nouă eră a îngrijirii personalizate a glaucomului. Deocamdată, menținerea informării despre stresul oxidativ și sănătatea cardiacă în glaucom este înțeleaptă. O nutriție bună, reducerea stresului și controalele regulate rămân esențiale pentru protejarea vederii dumneavoastră.