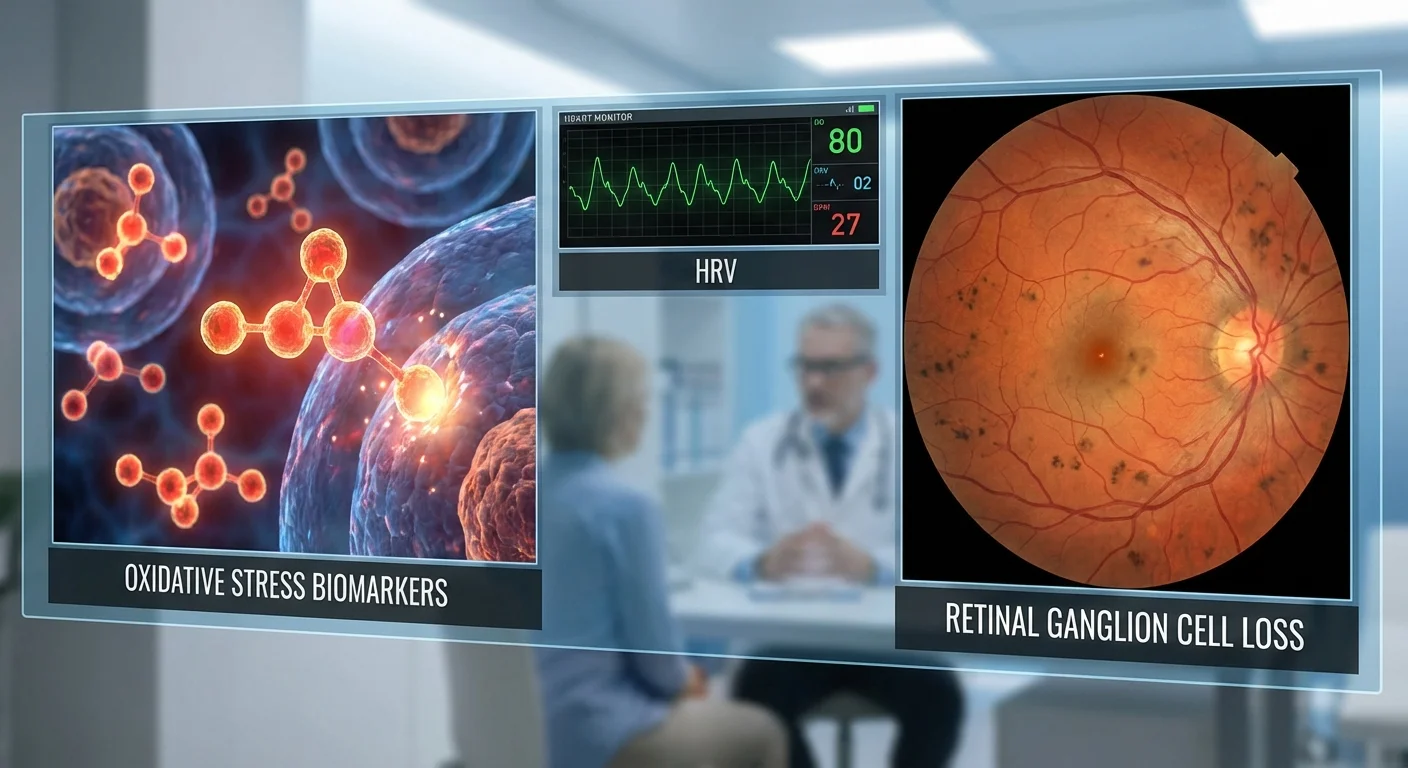
Giới thiệu
Bệnh tăng nhãn áp là một bệnh về mắt trong đó các tế bào hạch võng mạc (RGCs) – các tế bào thần kinh mang tín hiệu thị giác từ mắt đến não – chết dần. Điều này gây ra mất thị lực từ từ, không thể phục hồi. Các bác sĩ thường tập trung vào việc giảm áp lực mắt để làm chậm bệnh tăng nhãn áp, nhưng nghiên cứu hiện nay cho thấy stress oxy hóa (một loại căng thẳng hóa học trong cơ thể) và sự mất cân bằng trong hệ thần kinh tự chủ (hệ thần kinh “tự động” kiểm soát các chức năng như nhịp tim) cũng đóng một vai trò. Ở bệnh nhân tăng nhãn áp, nồng độ trong máu của một số chất chỉ điểm redox – các chất cho thấy tổn thương oxy hóa – có xu hướng cao hơn bình thường. Đồng thời, nhiều bệnh nhân tăng nhãn áp có biến thiên nhịp tim (HRV) suy giảm, một dấu hiệu của sự mất cân bằng tự chủ. Cùng với nhau, stress oxy hóa tăng cao và điều hòa tự chủ kém có thể làm tổn thương RGCs trầm trọng hơn.
Trong bài viết này, chúng tôi giải thích F2-isoprostanes, malondialdehyde (MDA) và 8-hydroxy-2’-deoxyguanosine (8-OHdG) là gì và cách chúng được tìm thấy trong bệnh tăng nhãn áp. Chúng tôi định nghĩa HRV (biến thiên nhịp tim) và xem xét cách nó bị thay đổi trong bệnh tăng nhãn áp. Chúng tôi mô tả các con đường sinh học có thể liên kết stress oxy hóa và mất cân bằng tự chủ với sự chết nhanh hơn của RGCs. Sau đó, chúng tôi tóm tắt những gì các nghiên cứu về chất chống oxy hóa (các chất dinh dưỡng chống lại stress oxy hóa) đã chỉ ra về kết quả bệnh tăng nhãn áp. Cuối cùng, chúng tôi đề xuất các nghiên cứu “đa omics” trong tương lai kết hợp các dấu ấn sinh học redox trong máu hoặc nước tiểu, các phép đo HRV và hình ảnh võng mạc tiên tiến để có được những hiểu biết mới.
Trong suốt bài viết, chúng tôi tập trung vào thông tin mà bệnh nhân có thể hiểu và thực hiện. Chúng tôi cũng giải thích các xét nghiệm stress oxy hóa nào có thể được chỉ định (qua máu hoặc nước tiểu) và các chỉ số cao hoặc thấp có thể có ý nghĩa gì đối với người quan tâm đến bệnh tăng nhãn áp.
Các Dấu Ấn Sinh Học của Stress Oxy Hóa trong Bệnh Tăng Nhãn Áp
Stress oxy hóa có nghĩa là có quá nhiều “gốc tự do” (các phân tử oxy phản ứng) trong cơ thể, gây tổn thương cho tế bào. Chúng ta không thể dễ dàng đo trực tiếp các gốc tự do, vì vậy các bác sĩ và nhà nghiên cứu sử dụng các dấu ấn sinh học trong máu hoặc nước tiểu để chỉ ra tổn thương oxy hóa. Ba dấu ấn quan trọng trong bệnh tăng nhãn áp là F2-isoprostanes, malondialdehyde (MDA) và 8-hydroxy-2’-deoxyguanosine (8-OHdG). Cả ba đều tăng lên khi stress oxy hóa gia tăng.
-
F2-Isoprostanes (8-iso-PGF2α) – đây là các phân tử ổn định được hình thành khi chất béo (chất béo không bão hòa đa trong màng tế bào) bị oxy hóa. F2-isoprostanes được coi là “tiêu chuẩn vàng” để đo quá trình oxy hóa lipid (chất béo) (pmc.ncbi.nlm.nih.gov). Nồng độ cao hơn trong máu hoặc nước tiểu của các chất này cho thấy các tế bào đang bị tấn công bởi quá trình oxy hóa. Mặc dù không phải tất cả các nghiên cứu về bệnh tăng nhãn áp đều đo chúng, nhưng mức F2-isoprostane cao đã được tìm thấy trong nhiều bệnh và được cho là phản ánh stress oxy hóa mạnh mẽ (pmc.ncbi.nlm.nih.gov). (Trong thực hành, các phòng thí nghiệm có thể đo F2-isoprostanes trong nước tiểu hoặc huyết tương bằng thiết bị chuyên dụng, nhưng điều này chủ yếu được thực hiện trong môi trường nghiên cứu.)
-
Malondialdehyde (MDA) – hóa chất này được tạo ra khi các loại oxy phản ứng phân hủy chất béo trong cơ thể. Giống như F2-isoprostanes, nó báo hiệu tổn thương chất béo do quá trình oxy hóa. Nhiều nghiên cứu về bệnh tăng nhãn áp đã phát hiện ra rằng bệnh nhân tăng nhãn áp có MDA trong máu cao hơn người khỏe mạnh (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Trên thực tế, một đánh giá lớn cho thấy MDA là dấu ấn stress oxy hóa được nâng cao nhất quán nhất trong máu bệnh nhân tăng nhãn áp (pmc.ncbi.nlm.nih.gov). Trong một nghiên cứu về bệnh tăng nhãn áp góc đóng, bệnh nhân có MDA cao hơn đáng kể so với nhóm đối chứng (pmc.ncbi.nlm.nih.gov). Đáng chú ý, nghiên cứu đó cho thấy bệnh nhân có mức MDA rất cao bị mất thị lực nhanh hơn: những người có MDA trên khoảng 12 đơn vị có sự suy giảm thị trường nhanh hơn nhiều (pmc.ncbi.nlm.nih.gov).
-
8-Hydroxy-2’-deoxyguanosine (8-OHdG) – dấu ấn này chỉ ra tổn thương oxy hóa đối với DNA (vật liệu di truyền trong tế bào). Khi stress oxy hóa cắt hoặc thay đổi DNA, mức 8-OHdG tăng lên và có thể được đo trong máu hoặc nước tiểu. Các nghiên cứu về bệnh nhân tăng nhãn áp (trong bệnh tăng nhãn áp áp lực bình thường và tăng nhãn áp bong bao giả) đã tìm thấy mức 8-OHdG trong huyết tương cao hơn đáng kể so với nhóm đối chứng (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Ví dụ, một nghiên cứu tìm thấy 8-OHdG trong máu trung bình khoảng 17 ng/mL ở người khỏe mạnh và ~23 ng/mL ở bệnh nhân tăng nhãn áp (pmc.ncbi.nlm.nih.gov). Một báo cáo khác cho thấy nguy cơ mắc bệnh tăng nhãn áp cao hơn 4 lần ở những người có 8-OHdG trên một mức giới hạn nhất định (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Tóm lại, 8-OHdG cao có nghĩa là DNA bị tổn thương nhiều hơn do oxy phản ứng, và điều này được thấy ở bệnh nhân tăng nhãn áp.
Các dấu ấn khác đôi khi được đo bao gồm tổng mức chất chống oxy hóa (như “tổng trạng thái chống oxy hóa” hoặc các enzyme như superoxide dismutase (SOD) và glutathione peroxidase). Trong nhiều nghiên cứu về bệnh tăng nhãn áp, các chất chống oxy hóa này thấp (vì chúng đã được sử dụng hết để chống lại các gốc tự do) trong khi các dấu ấn như MDA, 8-OHdG hoặc H₂O₂ cao (pmc.ncbi.nlm.nih.gov). (Để ngắn gọn, chúng tôi tập trung vào F2-isoprostanes, MDA và 8-OHdG ở đây, nhưng nhiều nghiên cứu báo cáo các enzyme và vitamin chống oxy hóa thấp hơn trong bệnh tăng nhãn áp.)
Tóm tắt: Ở bệnh nhân tăng nhãn áp, các nghiên cứu luôn thấy tổn thương oxy hóa cao hơn trong cơ thể. Các dấu ấn như MDA và 8-OHdG có xu hướng nằm ngoài phạm vi bình thường được thấy ở người khỏe mạnh (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Các nhà nghiên cứu tin rằng stress oxy hóa tăng thêm này góp phần vào tác động của bệnh tăng nhãn áp lên dây thần kinh thị giác.
Đo Stress Oxy Hóa: Các Xét Nghiệm Sẵn Có
Mặc dù các dấu ấn này quan trọng trong nghiên cứu, nhưng chúng chưa phải là các xét nghiệm lâm sàng thường quy. Tuy nhiên, một số phòng thí nghiệm chuyên biệt và phòng khám y tế cung cấp các bảng xét nghiệm stress oxy hóa. Dưới đây là những gì bệnh nhân nên biết:
-
Xét nghiệm 8-OHdG: Có thể được đo trong huyết tương máu hoặc trong nước tiểu. Các bộ kit thương mại (xét nghiệm ELISA) tồn tại để đo 8-OHdG trong nước tiểu (ví dụ, bộ kit Genox “8-OHdG Check” (www.genox.com)). Một nhà cung cấp dịch vụ chăm sóc sức khỏe có thể sắp xếp điều này thông qua các phòng thí nghiệm chuyên biệt. Không có mức “bình thường” phổ quát, nhưng các nghiên cứu đưa ra một số ý tưởng. Ví dụ, một nghiên cứu về bệnh tăng nhãn áp đã tìm thấy bệnh nhân đối chứng có mức trung bình ~17 ng/mL trong khi bệnh nhân tăng nhãn áp có mức trung bình ~23 ng/mL (pmc.ncbi.nlm.nih.gov). Nếu 8-OHdG của bạn cao hơn nhiều so với các giá trị bình thường điển hình, điều đó cho thấy tổn thương DNA tăng cao do stress oxy hóa.
-
Xét nghiệm F2-isoprostanes: Thường được đo trong mẫu nước tiểu 24 giờ hoặc đôi khi là máu. Nó được coi là rất đáng tin cậy nhưng yêu cầu thiết bị phòng thí nghiệm (phổ khối). Các giá trị bình thường phụ thuộc vào tuổi và phương pháp, nhưng một lần nữa kết quả cao hơn nhiều cho thấy quá trình peroxy hóa lipid tăng lên. Xét nghiệm này chủ yếu được thực hiện trong nghiên cứu hoặc các trung tâm chuyên biệt.
-
Xét nghiệm MDA: Malondialdehyde có thể được đo trong huyết tương máu (thường bằng phương pháp “các chất phản ứng với axit thiobarbituric” hoặc TBARS, hoặc bằng sắc ký). Các phạm vi phòng thí nghiệm bình thường khác nhau, nhưng một nghiên cứu về bệnh tăng nhãn áp đã sử dụng ngưỡng ~12 µmol/L để đánh dấu nguy cơ cao hơn (pmc.ncbi.nlm.nih.gov). Nếu báo cáo phòng thí nghiệm của bạn cho thấy MDA tăng cao hơn các giá trị điển hình (hãy hỏi phạm vi tham chiếu của phòng thí nghiệm), điều đó có thể chỉ ra stress oxy hóa quá mức đối với chất béo.
-
Các xét nghiệm tổng chất chống oxy hóa hoặc enzyme: Một số phòng thí nghiệm đo “tổng khả năng chống oxy hóa” hoặc mức SOD hoặc glutathione peroxidase. Kết quả thấp hơn bình thường một lần nữa chỉ ra stress oxy hóa, vì các chất chống oxy hóa đang được tiêu thụ.
Trong thực tế, các xét nghiệm này không phải là tiêu chuẩn như cholesterol hoặc đường huyết. Nếu bạn muốn kiểm tra chúng, bạn có thể cần yêu cầu một phòng thí nghiệm chuyên khoa hoặc tham khảo ý kiến bác sĩ có thể chỉ định chúng. Hãy lưu ý rằng kết quả phải được một chuyên gia diễn giải trong ngữ cảnh. Các yếu tố như chế độ ăn uống, thời gian trong ngày hoặc tập thể dục có thể ảnh hưởng đến các dấu ấn này.
Như một đánh giá đã chỉ ra, stress oxy hóa không được đánh giá thường quy trong thực hành hàng ngày (pmc.ncbi.nlm.nih.gov) vì bản thân các loại oxy phản ứng có thời gian tồn tại ngắn. Thay vào đó, các bác sĩ xem xét các dấu ấn gián tiếp (như trên) hoặc tập trung vào việc giảm căng thẳng thông qua lối sống. Nếu bạn nhận được kết quả xét nghiệm, hãy so sánh chúng với bất kỳ “phạm vi bình thường” nào được cung cấp và thảo luận với bác sĩ của bạn. Nói chung, 8-OHdG, MDA hoặc isoprostanes cao hơn bình thường cho thấy stress oxy hóa tăng lên, trong khi các mức trong phạm vi bình thường thì đáng yên tâm.
Chức Năng Tự Chủ và Biến Thiên Nhịp Tim trong Bệnh Tăng Nhãn Áp
Hệ thần kinh tự chủ (ANS) kiểm soát các chức năng không tự nguyện như nhịp tim, trương lực mạch máu và tiêu hóa. Nó có hai nhánh – giao cảm (thường được gọi là “chiến đấu hoặc bỏ chạy”) và đối giao cảm (nghỉ ngơi/tiêu hóa). Một sự cân bằng lành mạnh giữa chúng gây ra nhịp tim thay đổi liên tục. Biến thiên nhịp tim (HRV) là một thước đo mức độ dao động của thời gian giữa các nhịp tim. Nói một cách đơn giản, HRV cao hơn có nghĩa là tim đang phản ứng linh hoạt (thường là dấu hiệu của sức khỏe tốt), trong khi HRV rất thấp cho thấy mất cân bằng tự chủ, thường là quá nhiều hoạt động giao cảm hoặc trương lực đối giao cảm giảm.
Các nghiên cứu gần đây cho thấy bệnh nhân tăng nhãn áp thường có HRV giảm so với những người không mắc bệnh tăng nhãn áp (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Ví dụ, trong một nghiên cứu lớn, bệnh nhân mắc bệnh tăng nhãn áp bong bao giả (một dạng bệnh tăng nhãn áp góc mở) có các chỉ số HRV thấp hơn đáng kể so với nhóm đối chứng khỏe mạnh (pmc.ncbi.nlm.nih.gov). Một phân tích khác cho thấy bệnh nhân tăng nhãn áp có HRV thấp nhất (sự thống trị giao cảm mạnh nhất) có sự mỏng hóa lớp thần kinh thị giác trong võng mạc nhanh hơn nhiều so với những người có HRV cao hơn (pmc.ncbi.nlm.nih.gov). Trong nghiên cứu đó, nhóm HRV thấp mất khoảng 1,4 μm độ dày sợi thần kinh mỗi năm (so với chỉ 0,3 μm/năm ở nhóm HRV cao) (pmc.ncbi.nlm.nih.gov). Họ cũng có nhiều dao động áp lực mắt hơn và áp lực tưới máu mắt thấp hơn, cho thấy sự mất cân bằng tự chủ ảnh hưởng đến lưu lượng máu mắt.
Tóm lại, bệnh tăng nhãn áp – đặc biệt là một số loại như bệnh tăng nhãn áp bong bao giả – có xu hướng đi kèm với rối loạn chức năng ANS. Các nghiên cứu liên tục quan sát thấy rằng bệnh nhân tăng nhãn áp có sự thay đổi nhịp tim nhỏ hơn so với người khỏe mạnh (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). HRV thấp là một tín hiệu của stress mãn tính hoặc thần kinh giao cảm hoạt động quá mức. Quan trọng hơn, HRV thấp trong bệnh tăng nhãn áp đã được liên kết với kết quả xấu hơn: bệnh nhân có HRV suy giảm bị mất sợi thần kinh võng mạc nhanh hơn và nhiều khuyết tật thị trường trung tâm hơn (pmc.ncbi.nlm.nih.gov).
Đo HRV: Một người có thể đo HRV bằng các thiết bị như máy theo dõi nhịp tim hoặc thậm chí một số đồng hồ thông minh và điện thoại thông minh sử dụng cảm biến xung. Các phòng khám đôi khi sử dụng ECG ngắn hoặc máy phân tích HRV cầm tay (như cảm biến đầu ngón tay). Nếu HRV của bạn thấp hơn mức trung bình theo tuổi và giới tính, điều đó cho thấy stress tự chủ. Ví dụ, nghiên cứu [26] đã sử dụng SDNN (một thước đo HRV tiêu chuẩn) để chia bệnh nhân thành các nhóm HRV “thấp” và “cao”. Mặc dù không có ngưỡng đơn giản nào được công bố, nhưng SDNN dưới khoảng 50 ms thường được coi là thấp ở người lớn. Tuy nhiên, hãy tham khảo ý kiến bác sĩ với dữ liệu HRV thô; họ có thể sử dụng nó cùng với các thông tin sức khỏe khác chứ không phải một mình.
Liên kết với Stress Oxy Hóa: HRV thấp có nghĩa là cơ thể đang ở trạng thái căng thẳng cao hơn. Trong nhiều tình trạng (như bệnh thận mãn tính hoặc bệnh tim), các nhà nghiên cứu đã phát hiện ra rằng các dấu ấn sinh học stress oxy hóa cao hơn đi đôi với HRV thấp hơn (pmc.ncbi.nlm.nih.gov). Trong một nghiên cứu về bệnh nhân bệnh thận, những người có mức F2-isoprostane trong huyết tương cao (một thước đo stress oxy hóa) có HRV giảm đáng kể (pmc.ncbi.nlm.nih.gov). Mặc dù mối liên kết chính xác này chưa được nghiên cứu rộng rãi trong bệnh tăng nhãn áp, nhưng nó gợi ý một vòng luẩn quẩn: stress oxy hóa có thể ảnh hưởng đến mạch máu và thần kinh, dẫn đến mất cân bằng tự chủ, từ đó có thể làm trầm trọng thêm lưu lượng máu và stress lên mắt.
Stress Oxy Hóa và Mất Cân Bằng Tự Chủ Có Thể Đẩy Nhanh Sự Mất RGCs Như Thế Nào
Để hiểu cách stress oxy hóa và mất cân bằng ANS có thể khiến các tế bào hạch võng mạc (RGCs) chết nhanh hơn, hãy xem xét các con đường liên quan này:
-
Tổn thương oxy hóa trực tiếp đến RGCs: RGCs là các tế bào thần kinh có nhu cầu năng lượng rất cao (đặc biệt là các sợi trục không myelin dài của chúng bên trong võng mạc) (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Chúng phụ thuộc rất nhiều vào ty thể (nhà máy năng lượng của tế bào) để sản xuất ATP. Ty thể tự nhiên giải phóng các loại oxy phản ứng (ROS) trong quá trình sản xuất năng lượng. Nếu sản xuất ROS quá cao hoặc hệ thống phòng thủ chống oxy hóa của tế bào yếu, ROS dư thừa sẽ tích tụ. Ở RGCs, điều này có nghĩa là tổn thương oxy hóa đối với DNA, protein và lipid. Ví dụ, 8-OHdG được hình thành khi ROS làm hỏng DNA trong RGCs. Một khi DNA và màng ty thể bị tổn thương, các quá trình tế bào quan trọng sẽ thất bại. ROS cao mãn tính kích hoạt chương trình tự hủy của tế bào (apoptosis) bằng cách giải phóng các yếu tố như cytochrome c từ ty thể (pmc.ncbi.nlm.nih.gov). Nói một cách đơn giản, quá nhiều stress oxy hóa đầu độc RGCs và khiến chúng tự hủy diệt. Điều này đã được thấy trong nhiều nghiên cứu về mắt: ROS dư thừa được tìm thấy trong các tế bào võng mạc sau chấn thương, và việc thêm chất chống oxy hóa có thể ngăn chặn tổn thương trong các mô hình động vật (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov).
-
Tác động mạch máu (lưu lượng máu): Mất cân bằng tự chủ (hoạt động giao cảm quá mức) có thể làm hẹp mạch máu và giảm lưu lượng máu đến mắt. Trong bệnh tăng nhãn áp, cung cấp máu đầy đủ là rất quan trọng cho sự sống sót của RGCs. Ví dụ, nghiên cứu [26] cho thấy bệnh nhân có HRV thấp có áp lực tưới máu mắt (áp lực máu hiệu quả cung cấp cho dây thần kinh thị giác) thấp hơn và nhiều dao động áp lực mắt hơn theo năm. Huyết áp thấp hoặc áp lực mắt tăng đột biến có thể làm RGCs thiếu oxy liên tục. Thiếu máu cục bộ (thiếu oxy) bản thân nó gây ra stress oxy hóa – khi nguồn cung cấp oxy trở lại, nó tạo ra ROS (tổn thương thiếu máu cục bộ-tái tưới máu). Do đó, co mạch do ANS và sự bất ổn định lưu lượng máu tạo ra một vòng tuần hoàn thiếu oxy và tổn thương oxy hóa cho RGCs (pmc.ncbi.nlm.nih.gov).
-
Viêm và stress tế bào: Stress oxy hóa có thể làm viêm các tế bào hỗ trợ trong võng mạc (tế bào thần kinh đệm). Các tế bào này sau đó giải phóng các phân tử gây viêm làm tăng thêm stress lên RGCs. Trong khi đó, rối loạn chức năng tự chủ thường được liên kết với tình trạng viêm mức độ thấp toàn thân. Cùng với nhau, ROS quá mức và trạng thái giao cảm có thể làm tăng cường tình trạng viêm có hại xung quanh đầu dây thần kinh thị giác, đẩy nhanh sự chết của RGCs.
-
Tương tác stress cơ học: Áp lực mắt cao (IOP) bản thân nó làm biến dạng đầu dây thần kinh thị giác, kéo căng các sợi trục RGC. Các sợi trục bị stress trở nên thiếu năng lượng và sản xuất nhiều ROS hơn. Nếu chất chống oxy hóa thấp (như thấy ở bệnh nhân tăng nhãn áp), ROS dư thừa sẽ làm mất cân bằng dẫn đến chết tế bào. Mất cân bằng ANS có thể làm trầm trọng thêm sự dao động IOP và giảm khả năng điều hòa IOP và lưu lượng máu của mắt, làm tăng cường tác động này (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov).
Tóm lại, stress oxy hóa làm hỏng RGCs ở cấp độ tế bào, trong khi các vấn đề về mạch máu tự chủ/tự chủ làm suy giảm cung cấp máu và khả năng chữa lành của RGCs. Một đánh giá lớn về bệnh tăng nhãn áp đã tóm tắt ngắn gọn: quá trình chết tế bào RGC trong bệnh tăng nhãn áp được thúc đẩy bởi IOP tăng cao, lưu lượng máu kém (“suy giảm mạch máu”) và stress oxy hóa (pmc.ncbi.nlm.nih.gov). Các yếu tố này hoạt động cùng nhau: stress oxy hóa làm tổn thương ty thể và DNA của RGC (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov), trong khi stress tự chủ gây ra thiếu máu cục bộ võng mạc và thiếu chất dinh dưỡng, dẫn đến chết tế bào RGC nhanh hơn. Ở bệnh nhân, điều này thể hiện là mất sợi thần kinh thị giác và thị lực nhanh hơn khi HRV thấp (pmc.ncbi.nlm.nih.gov) hoặc các dấu ấn oxy hóa cao (pmc.ncbi.nlm.nih.gov).
Can Thiệp Chống Oxy Hóa và Kết Quả Bệnh Tăng Nhãn Áp
Bởi vì bệnh tăng nhãn áp liên quan đến tổn thương oxy hóa, nhiều nghiên cứu đã đặt câu hỏi liệu thực phẩm bổ sung chống oxy hóa có thể giúp bảo vệ mắt hay không. Các chất chống oxy hóa bao gồm vitamin (C, E), các chất dinh dưỡng như coenzyme Q10, flavonoid (trong trái cây/trà), axit béo omega-3 và chiết xuất thực vật (như Gingko biloba). Các chất này có thể trung hòa các gốc tự do, ít nhất là trên lý thuyết.
Kết quả thí nghiệm và trên động vật: Trong các mô hình động vật mắc bệnh tăng nhãn áp hoặc tổn thương mắt, việc bổ sung chất chống oxy hóa thường làm giảm sự mất RGC. Ví dụ, ở chuột với bệnh tăng nhãn áp hoặc thiếu máu cục bộ võng mạc, các chất bổ sung như vitamin A, Ginkgo, axit alpha-lipoic, coenzyme Q10, axit béo omega-3 và resveratrol đều cho thấy một số tác dụng bảo vệ tế bào võng mạc (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Bảng của một đánh giá liệt kê nhiều thí nghiệm: ví dụ, chiết xuất Ginkgo biloba làm giảm chết RGC ở mắt chuột có áp lực cao (pmc.ncbi.nlm.nih.gov); coenzyme Q10 và vitamin E bảo vệ các tế bào võng mạc được nuôi cấy khỏi độc tố oxy hóa (pmc.ncbi.nlm.nih.gov); và các chất chống oxy hóa trong chế độ ăn uống (như anthocyanin từ trái cây) giúp bảo tồn cấu trúc võng mạc trong các mô hình bệnh tăng nhãn áp trên động vật (pmc.ncbi.nlm.nih.gov). Các nghiên cứu này gợi ý rằng các chất chống oxy hóa có thể giúp các tế bào võng mạc sống sót qua stress.
Thử nghiệm lâm sàng trên người: Các thử nghiệm trên bệnh nhân tăng nhãn áp đã nhỏ hơn và có kết quả hỗn hợp, nhưng một số thì đáng khích lệ. Một đánh giá hệ thống gần đây gồm 15 thử nghiệm ngẫu nhiên cho thấy các chất bổ sung chống oxy hóa cải thiện đáng kể các kết quả liên quan đến bệnh tăng nhãn áp (pmc.ncbi.nlm.nih.gov). Trung bình, bệnh nhân dùng chất chống oxy hóa (vitamin, coenzyme Q10, lutein, v.v.) có áp lực mắt thấp hơn, mất thị trường chậm hơn và lưu lượng máu mắt tốt hơn so với những người dùng giả dược (pmc.ncbi.nlm.nih.gov). Quan trọng là không có thêm tác dụng phụ nào (như thay đổi huyết áp) ở nhóm dùng chất chống oxy hóa so với giả dược, vì vậy chúng có vẻ an toàn (pmc.ncbi.nlm.nih.gov).
Một số phát hiện cụ thể trên người: trong một thử nghiệm năm 2003, bệnh nhân tăng nhãn áp dùng chiết xuất Ginkgo biloba có những cải thiện khiêm tốn về chỉ số thị trường (pmc.ncbi.nlm.nih.gov). Một nghiên cứu sau đó xác nhận rằng bệnh nhân NVG (bệnh tăng nhãn áp áp lực bình thường) dùng Gingko có lưu lượng máu tốt hơn quanh dây thần kinh thị giác (pmc.ncbi.nlm.nih.gov). Các thử nghiệm nhỏ khác cho thấy lợi ích của chiết xuất trà xanh (epigallocatechin gallate) đối với chức năng võng mạc, hoặc anthocyanin từ quả lý chua đen giúp tăng cường tuần hoàn mắt (mặc dù IOP hoặc thị lực không thay đổi nhiều) (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Một sự kết hợp của các chiết xuất thực vật (forskolin+rutin) thậm chí còn làm giảm IOP khoảng 10% so với việc chỉ dùng thuốc nhỏ mắt thông thường (pmc.ncbi.nlm.nih.gov).
Tuy nhiên, công bằng mà nói, kết quả rất đa dạng. Một số thử nghiệm chống oxy hóa cho thấy những cải thiện khiêm tốn hoặc không có. Sự khác biệt về liều lượng, loại bệnh nhân và quy mô nghiên cứu đều quan trọng. Nhìn chung, hầu hết bằng chứng cho thấy việc bổ sung chất chống oxy hóa là hứa hẹn và an toàn, nhưng chưa phải là một phương pháp chữa trị độc lập. Các đánh giá lớn kết luận rằng chúng có thể giúp làm chậm tổn thương do bệnh tăng nhãn áp (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov), nhưng các nghiên cứu lớn hơn, dứt khoát hơn vẫn cần thiết.
Điểm cốt lõi thực tế: Ít nhất, một chế độ ăn uống lành mạnh giàu chất chống oxy hóa (trái cây, rau xanh lá, omega-3) có vẻ là khôn ngoan cho sức khỏe mắt. Một số bác sĩ nhãn khoa đã khuyến nghị bổ sung các vitamin như C/E, lutein, hoặc omega-3 cho bệnh nhân tăng nhãn áp như một biện pháp bổ sung. Hãy kiểm tra với bác sĩ của bạn trước khi bắt đầu bất kỳ loại thuốc nào, đặc biệt là ở liều cao. Nghiên cứu cho đến nay ngụ ý rằng các chất bổ sung như vậy sẽ không gây hại và có thể giúp ích cho các khía cạnh của bệnh tăng nhãn áp như lưu lượng máu hoặc sức khỏe thần kinh (pmc.ncbi.nlm.nih.gov).
Hướng Đi Tương Lai: Tích Hợp Redox, HRV và Hình Ảnh Võng Mạc
Các nhà nghiên cứu hiện đang hình dung các nghiên cứu tích hợp hơn – được gọi là đa omics – để vượt qua bệnh tăng nhãn áp. Điều này có nghĩa là thu thập nhiều loại dữ liệu cùng lúc: các dấu ấn trong máu (hoặc nước tiểu) về cân bằng redox, ghi nhận HRV liên tục, hình ảnh võng mạc chi tiết, và thậm chí cả hồ sơ di truyền hoặc trao đổi chất. Bằng cách ghép tất cả các mảnh lại với nhau, người ta có thể tìm thấy các mẫu không thể nhìn thấy khi riêng lẻ.
Ví dụ, phân tích trao đổi chất hiện đại (đo hàng chục phân tử nhỏ trong máu) đã tiết lộ những dấu hiệu độc đáo trong bệnh tăng nhãn áp. Một đánh giá về các nghiên cứu trao đổi chất trên người đã tìm thấy mức axit amin, lipid và các con đường liên quan bị thay đổi ở bệnh nhân tăng nhãn áp (pmc.ncbi.nlm.nih.gov). Những thay đổi trao đổi chất này gợi ý các quá trình cơ bản có thể được nhắm mục tiêu. Kết hợp điều đó với dữ liệu HRV (tương tác ruột-não-ANS) và hình ảnh OCT độ phân giải cao của dây thần kinh thị giác và các lớp võng mạc, các nhà nghiên cứu có thể phân loại bệnh nhân thành các nhóm nhỏ. Có lẽ một số bệnh nhân có hồ sơ “stress oxy hóa cao” (8-OHdG rất cao, HRV thấp và lớp sợi thần kinh võng mạc mỏng hơn trên OCT), trong khi những người khác thì không.
Một ví dụ song song có thể thấy trong nghiên cứu về bệnh võng mạc tiểu đường: một nghiên cứu gần đây trên chuột đã sử dụng phương pháp đa omics, kết hợp phân tích biểu hiện gen mô võng mạc, phân tích trao đổi chất huyết thanh máu và dữ liệu di truyền (GWAS), để liên kết những thay đổi chất chuyển hóa trong máu với viêm võng mạc sớm (pmc.ncbi.nlm.nih.gov). Áp dụng một chiến lược tương tự cho bệnh tăng nhãn áp – ví dụ, liên kết chuyển hóa ngoại vi với sự mất sợi thần kinh võng mạc – có thể khám phá các mục tiêu thuốc hoặc dấu ấn sàng lọc mới. Chẳng hạn, nếu một số chất chuyển hóa trong máu tăng đều đặn trước khi có bất kỳ mất thị lực nào, chúng có thể trở thành các dấu ấn sinh học cảnh báo sớm.
Điều này có ý nghĩa gì đối với bệnh nhân: Trong tương lai, một lần khám bệnh có thể bao gồm một bảng xét nghiệm máu (hoặc nước tiểu) đơn giản để tìm một số dấu ấn stress oxy hóa, một phép đo HRV (như ECG năm phút hoặc thiết bị đeo theo dõi tại nhà) và hình ảnh mắt tiên tiến. Phân tích tất cả các kết quả cùng nhau có thể dự đoán ai có nguy cơ tiến triển cao nhất. Hơn nữa, nếu một dấu ấn sinh học cụ thể (chẳng hạn, F2-isoprostanes rất cao) được phát hiện là nguyên nhân gây tổn thương, người ta có thể điều chỉnh điều trị để giảm stress đó hoặc sử dụng các chất chống oxy hóa nhắm mục tiêu.
Hiện tại, chúng ta chưa đạt được điều đó, nhưng nghiên cứu đa omics về bệnh tăng nhãn áp là một hướng đi hứa hẹn. Hy vọng là sẽ vượt ra ngoài việc chỉ tập trung vào áp lực mắt và xây dựng một bức tranh đầy đủ hơn về bệnh của mỗi bệnh nhân.
Kết Luận
Bệnh tăng nhãn áp không chỉ là áp lực mắt cao – nó còn liên quan đến stress oxy hóa lan rộng trong cơ thể và rối loạn chức năng của hệ thần kinh tự chủ. Bệnh nhân tăng nhãn áp có xu hướng có mức dấu ấn máu cao hơn như MDA và 8-OHdG, cho thấy tổn thương tế bào và DNA (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Đồng thời, họ thường cho thấy biến thiên nhịp tim suy giảm, phản ánh sự kích hoạt quá mức của hệ giao cảm (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Hai yếu tố này có khả năng hoạt động cùng nhau để tiêu diệt các tế bào hạch võng mạc nhanh hơn. Stress oxy hóa làm hỏng ty thể và DNA của RGC (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov), trong khi mất cân bằng tự chủ dẫn đến lưu lượng máu mắt kém và dao động áp lực (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov).
Có bằng chứng tốt cho thấy chất chống oxy hóa có thể giúp ích – các nghiên cứu trên động vật luôn cho thấy sự bảo vệ RGC (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov), và các thử nghiệm trên người chỉ ra rằng các chất bổ sung có thể cải thiện thị trường và lưu lượng máu mắt (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Bệnh nhân có thể thảo luận về các vitamin và chất dinh dưỡng chống oxy hóa với bác sĩ nhãn khoa của mình như một phần của cách tiếp cận lối sống lành mạnh.
Quan trọng là, một số xét nghiệm stress oxy hóa (8-OHdG, MDA, isoprostanes trong máu hoặc nước tiểu) có thể tiếp cận được, mặc dù không phải là thường quy. Nếu các xét nghiệm này được đo, các giá trị tăng cao (như 8-OHdG cao hơn nhiều so với ~20 ng/mL hoặc MDA trên các phạm vi phòng thí nghiệm đã biết) nên thúc đẩy sự chú ý đến chế độ ăn uống, lối sống và có thể là hỗ trợ chống oxy hóa. Tương tự, đo HRV (bằng máy theo dõi đơn giản tại nhà hoặc ECG tại phòng khám) có thể chỉ ra sức khỏe tự chủ; HRV thấp có thể có nghĩa là mắt đang chịu thêm căng thẳng.
Trong tương lai, việc kết hợp các phép đo này với hình ảnh võng mạc tiên tiến và dữ liệu di truyền trong các nghiên cứu tích hợp có thể mở ra một kỷ nguyên mới của chăm sóc bệnh tăng nhãn áp cá nhân hóa. Hiện tại, việc cập nhật thông tin về stress oxy hóa và sức khỏe tim mạch trong bệnh tăng nhãn áp là khôn ngoan. Dinh dưỡng tốt, giảm căng thẳng và khám sức khỏe định kỳ vẫn là chìa khóa để bảo vệ thị lực của bạn.