นิโคตินาไมด์กับการช่วยฟื้นฟูไมโทคอนเดรีย: การบำบัดเมตาบอลิซึมสามารถฟื้นฟูการทำงานได้หรือไม่?
โรคต้อหินเป็นสาเหตุสำคัญของการสูญเสียการมองเห็นอย่างถาวร ซึ่งมักดำเนินไปแม้จะสามารถควบคุมความดันในลูกตา (IOP) ได้แล้วก็ตาม หลักฐานที่เพิ่มขึ้นชี้ให้เห็นว่า เซลล์ปมประสาทจอประสาทตา (RGCs) มีความเปราะบางเป็นพิเศษต่อความเครียดทางเมตาบอลิซึม โดยเฉพาะอย่างยิ่งจากการพร่องของนิโคตินาไมด์อะดีนีนไดนิวคลีโอไทด์ (NAD+) อย่างเรื้อรัง ซึ่งเป็นโคเอนไซม์ที่จำเป็นต่อการผลิตพลังงานของไมโทคอนเดรีย (pmc.ncbi.nlm.nih.gov). ดังนั้น นิโคตินาไมด์ (NAM) ซึ่งเป็นวิตามินบี 3 รูปแบบหนึ่งและเป็นสารตั้งต้นของ NAD+ จึงได้กลายเป็นแนวทางการบำบัดที่ช่วยปกป้องระบบประสาทที่มีแนวโน้มดี จากการศึกษาในแบบจำลองสัตว์และการศึกษาในมนุษย์ช่วงแรก การเสริม NAM แสดงให้เห็นถึงการรักษาสภาพและความสามารถในการทำงานของ RGCs ได้อย่างมีนัยสำคัญ (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). บทความนี้จะทบทวนการทดลองทางคลินิกแบบสุ่มล่าสุดของการใช้นิโคตินาไมด์ (NAM) ในปริมาณสูง (ร่วมกับไพรูเวทหรือไม่ก็ได้) และหารือว่าการเติม NAD+ อาจ “ช่วยฟื้นฟู” เซลล์ RGCs ที่ประสบภาวะเครียดแต่ยังคงอยู่รอดได้อย่างไร นอกจากนี้ยังครอบคลุมถึงข้อพิจารณาในการให้ยา ความปลอดภัย ความหลากหลายของการตอบสนอง การคัดเลือกผู้ป่วย และการวิจัยที่กำลังดำเนินอยู่
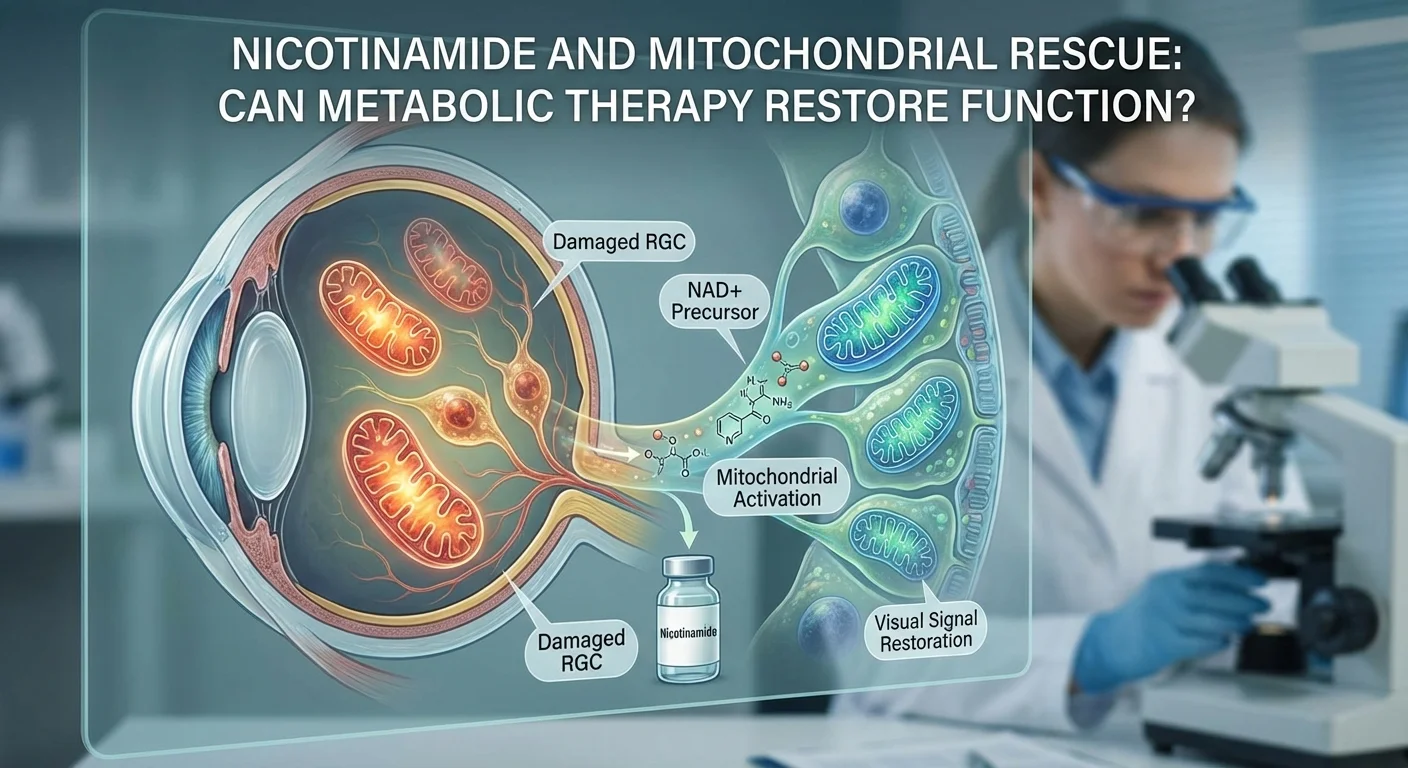
พื้นฐานทางเมตาบอลิซึมของโรคต้อหินและการเติม NAD+
เซลล์ RGCs มีความต้องการทางเมตาบอลิซึมสูงมาก และพึ่งพาการทำงานของไมโทคอนเดรียที่แข็งแรง ในโรคต้อหิน อายุที่มากขึ้นและความเครียดเรื้อรังเป็นตัวกระตุ้นให้เกิดการพร่องของ NAD+ ในเซลล์ RGCs อย่างต่อเนื่อง NAD+ เป็นโคแฟกเตอร์สำคัญในการสังเคราะห์พลังงานโดยอาศัยออกซิเจน (oxidative phosphorylation) และในวิถีการทำงานต่างๆ (เช่น เซอร์ทูอินและกระบวนการซ่อมแซม DNA) ที่ช่วยสนับสนุนการรอดชีวิตของเซลล์ (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). เมื่อระดับ NAD+ ลดลง เซลล์ RGCs จะประสบภาวะความล้มเหลวทางชีวพลังงาน ความเครียดจากปฏิกิริยาออกซิเดชันที่สูงขึ้น และความเสี่ยงต่อการเกิดอะพอพโทซิส (การตายของเซลล์แบบตั้งโปรแกรม) การเสริมนิโคตินาไมด์สามารถเติม NAD+ ได้ผ่านวิถี NAD+ salvage สิ่งนี้ช่วยรักษากระบวนการผลิต ATP ของไมโทคอนเดรียและกระตุ้นเอนไซม์ที่ช่วยให้เซลล์รอด (เช่น SIRT1) ในขณะที่ป้องกันการทำงานเกินของ PARP1 (เอนไซม์ซ่อมแซม DNA ที่อาจทำให้ NAD+ ลดลงได้) (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov).
กล่าวโดยสรุป การฟื้นฟู NAD+ อาจ กระตุ้นเซลล์ RGCs ที่ “ไม่ทำงาน” ให้กลับมามีชีวิตชีวา ตัวอย่างเช่น การศึกษา อิเล็กโทรเรตินนิกราฟี แสดงให้เห็นว่าผู้ป่วยต้อหินที่ได้รับ NAM มีแอมพลิจูดของการตอบสนองเชิงลบแบบโฟโตปิก (PhNR) ที่ใหญ่ขึ้น ซึ่งเป็นมาตรวัดเชิงวัตถุประสงค์ของการทำงานของจอประสาทตาชั้นใน (RGC) เมื่อเทียบกับกลุ่มที่ได้รับยาหลอก (pmc.ncbi.nlm.nih.gov). การศึกษาเหล่านี้ชี้ให้เห็นว่า NAM ป้องกันการทำงานผิดปกติของไมโทคอนเดรียในระยะแรก และสามารถกระตุ้นการทำงานของ RGCs ได้แม้หลังจากเริ่มมีอาการของโรค ในแบบจำลองโรคต้อหินในสัตว์ นิโคตินาไมด์ในปริมาณสูงช่วยรักษารูปร่างของ RGCs ได้อย่างแข็งแกร่งและป้องกันการสูญเสียการมองเห็น (pmc.ncbi.nlm.nih.gov). โดยรวมแล้ว การค้นพบเหล่านี้สนับสนุนแนวคิดที่ว่าเซลล์ RGCs ที่ประสบภาวะเครียดแต่ยังไม่ตาย สามารถถูก “ฟื้นฟู” ทางเมตาบอลิซึมได้ด้วยการเติม NAD+
หลักฐานจากการทดลองทางคลินิกสำหรับนิโคตินาไมด์
การทดลองแบบสุ่มล่าสุดหลายครั้งได้ทดสอบนิโคตินาไมด์ในปริมาณสูง (ร่วมกับไพรูเวทหรือไม่ก็ได้) ในผู้ป่วยต้อหิน ผลลัพธ์สำคัญที่ประเมินได้แก่ การตรวจทางสรีรวิทยาไฟฟ้า (pattern หรือ photopic ERG) และการทดสอบการทำงานของการมองเห็น (visual field)
-
การเสริมนิโคตินาไมด์เพียงอย่างเดียว (ปริมาณสูง): การทดลองแบบครอสโอเวอร์ในออสเตรเลียได้สุ่มผู้ป่วยต้อหินมุมเปิดปฐมภูมิที่ได้รับการรักษาจำนวน 57 ราย ให้ได้รับ NAM ในปริมาณสูง (1.5 กรัม/วัน เป็นเวลา 6 สัปดาห์ จากนั้น 3.0 กรัม/วัน เป็นเวลา 6 สัปดาห์) เทียบกับยาหลอก จากนั้นสลับกลุ่มกัน (www.researchgate.net). ในการศึกษานี้ การทำงานของจอประสาทตาชั้นในดีขึ้นอย่างมีนัยสำคัญเมื่อได้รับ NAM แอมพลิจูดของ PhNR (Vmax) เพิ่มขึ้นประมาณ 14.8% ในกลุ่มที่ได้รับ NAM (เทียบกับ 5.2% ในกลุ่มยาหลอก, p=0.02) และอัตราส่วน PhNR/b-wave เพิ่มขึ้นประมาณ 12.6% ในกลุ่มที่ได้รับ NAM (p=0.002) (www.researchgate.net). ที่น่าสังเกตคือ 23% ของผู้ป่วยที่ได้รับ NAM แสดงให้เห็นการพัฒนาของ PhNR ที่เกินกว่าความผันผวนตามธรรมชาติ เทียบกับเพียง 9% ในกลุ่มยาหลอก (www.researchgate.net). นอกจากนี้ยังมีแนวโน้มว่าลานสายตาดีขึ้น: 27% ของดวงตาดีขึ้น ≥1 dB ในค่าเบี่ยงเบนเฉลี่ยเมื่อได้รับ NAM เทียบกับเพียง 4% ในกลุ่มยาหลอก (p=0.02) (www.researchgate.net). การปฏิบัติตามคำแนะนำเป็นไปอย่างดีเยี่ยม (>94%) และ NAM ได้รับการยอมรับได้ดี ผลลัพธ์เหล่านี้ชี้ให้เห็นว่า NAM เพียงอย่างเดียวสามารถ ปรับปรุงมาตรวัดเชิงวัตถุประสงค์ของการทำงานของ RGC ได้ภายในไม่กี่เดือน แม้จะไม่มีการลด IOP ก็ตาม (www.researchgate.net).
-
นิโคตินาไมด์บวกไพรูเวท: ในการทดลองระยะที่ 2 (JAMA Ophthalmology 2021) ผู้ป่วยต้อหิน 57 รายถูกสุ่มให้ได้รับนิโคตินาไมด์ (1.5 กรัม/วัน เป็นเวลา 6 สัปดาห์ จากนั้น 3.0 กรัม/วัน เป็นเวลา 6 สัปดาห์) ร่วมกับแคลเซียมไพรูเวท เทียบกับยาหลอก (pmc.ncbi.nlm.nih.gov). การศึกษานี้ประเมินการตรวจลานสายตาด้วยเครื่องอัตโนมัติมาตรฐาน (SAP) ตลอดระยะเวลาการรักษาประมาณ 2 เดือน กลุ่มที่ได้รับ NAM+ไพรูเวทมีตำแหน่งลานสายตาที่ดีขึ้นมากกว่ากลุ่มยาหลอกอย่างมีนัยสำคัญ อันที่จริง ดวงตาที่ได้รับการรักษามีโอกาสสามเท่าที่จะมีการปรับปรุงความไวแบบจุดต่อจุด (pmc.ncbi.nlm.nih.gov). ความปลอดภัยอยู่ในระดับดี ที่สำคัญคือ การปรับปรุงมักจะเกิดขึ้นในบริเวณที่มี การสูญเสียลานสายตาเล็กน้อยหรือปานกลาง ไม่ใช่ในบริเวณที่เสียหายรุนแรงหรือตายแล้ว (pmc.ncbi.nlm.nih.gov). สิ่งนี้ชี้ให้เห็นว่าการบำบัดเมตาบอลิซึมช่วยฟื้นฟูเซลล์ RGCs ที่ “เครียดแต่ยังไม่ตาย” ทำให้ได้ผลการตรวจลานสายตาและ ERG ที่ดีขึ้น (pmc.ncbi.nlm.nih.gov). สอดคล้องกับการทดลองที่ใช้ NAM เพียงอย่างเดียว การศึกษานี้บ่งชี้ถึงประโยชน์ด้านการทำงานในระยะสั้นจากการเติม NAD+ แม้ว่ามาตรวัดโครงสร้าง (เช่น ความหนาของ OCT RNFL) จะไม่เปลี่ยนแปลงก็ตาม
สรุปได้ว่า การทดลองทั้งสองแสดงให้เห็นถึงการปรับปรุงการทำงาน ในผู้ป่วยต้อหินที่ได้รับ NAM การทดลองครอสโอเวอร์ของออสเตรเลีย (NAM เทียบกับยาหลอก) พบว่า PhNR เพิ่มขึ้นอย่างมีนัยสำคัญทางสถิติ และมีแนวโน้มที่ดีขึ้นในค่า MD ของลานสายตา (www.researchgate.net). การทดลอง JAMA (NAM+ไพรูเวท) แสดงให้เห็นจุดในลานสายตาที่ดีขึ้นเมื่อได้รับการรักษา (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). ผลกระทบโดยทั่วไปอยู่ในระดับปานกลางและสังเกตได้ภายในไม่กี่สัปดาห์ จำเป็นต้องมีการทดลองขนาดใหญ่ขึ้นและนานขึ้นเพื่อประเมินความคงทนของผลลัพธ์
กลไก: การ “ช่วยฟื้นฟู” เซลล์ RGCs ที่ยังคงมีชีวิต
NAM สร้างประโยชน์เหล่านี้ได้อย่างไร? แนวคิดสำคัญคือเซลล์ RGCs ที่ ไม่ทำงาน หรือ เครียด ในโรคต้อหิน เซลล์ RGCs บางส่วนมีการทำงานของเมตาบอลิซึมที่บกพร่องแต่ยังคงมีชีวิตอยู่ ด้วยการเพิ่ม NAD+ นั้น NAM สามารถกระตุ้นการผลิต ATP ของไมโทคอนเดรียในเซลล์เหล่านี้ได้ ซึ่งจะช่วยปรับปรุงการส่งสัญญาณและการทำงานของไซแนปส์ (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). เอกสารของ JAMA สังเกตว่าการปรับปรุงการมองเห็นส่วนใหญ่เกิดขึ้นในตำแหน่งการทดสอบที่มีการสูญเสียความไวเล็กน้อยถึงปานกลาง มักจะอยู่บริเวณขอบของสโคโตมา (จุดบอดในลานสายตา) (pmc.ncbi.nlm.nih.gov). ในทางตรงกันข้าม บริเวณที่เสียหายรุนแรง (ซึ่งเซลล์ RGCs น่าจะสูญเสียไปอย่างถาวรแล้ว) ไม่มีการปรับปรุง กล่าวอีกนัยหนึ่ง NAM ดูเหมือนจะ ดึง เซลล์ RGCs ที่เสื่อมสภาพบางส่วนให้กลับมาทำงานได้อีกครั้ง นอกจากนี้ การรวม NAM เข้ากับไพรูเวท (ซึ่งเป็นสารตั้งต้นพลังงาน) อาจช่วยเสริมการสนับสนุนเมตาบอลิซึมในหลายด้าน
ในระดับโมเลกุล การเพิ่มขึ้นของ NAD+ สามารถกระตุ้นวิถีทางที่ช่วยปกป้องระบบประสาทได้ ตัวอย่างเช่น เซอร์ทูอิน-1 (SIRT1) ต้องการ NAD+ เพื่อทำหน้าที่ดีแอซีทิเลทเอนไซม์ไมโทคอนเดรียและสนับสนุนการต้านทานความเครียด ในขณะที่โพลี-เอดีพี-ไรโบส พอลิเมอเรส-1 (PARP-1) จะใช้ NAD+ เมื่อทำงานเกินปกติในช่วงที่เกิดความเสียหายของ DNA ด้วยการเสริมปริมาณ NAD+ นั้น NAM สามารถรักษากิจกรรมของ SIRT1 และจำกัดการตายของเซลล์ที่เกิดจาก PARP ได้ การศึกษาในสัตว์หลายชิ้นยืนยันว่าการเสริม NAM ช่วยให้สุขภาพของไมโทคอนเดรียมีเสถียรภาพ รักษากิ่งแขนงประสาทของ RGCs และคงสภาพความสมบูรณ์ของเส้นประสาทตาไว้ได้ (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). บทความทบทวนฉบับหนึ่งระบุว่า NAM “เพิ่มระดับ NAD+ ป้องกันความผิดปกติของไมโทคอนเดรียในระยะแรก และเพิ่มแอมพลิจูดของการตอบสนองเชิงลบแบบโฟโตปิก” ในต้อหินจากการทดลอง (pmc.ncbi.nlm.nih.gov). ดังนั้น การเติม NAD+ จึงเป็นกลไกที่เป็นไปได้สำหรับการปรับปรุงที่สังเกตได้ทางคลินิก
ข้อพิจารณาในการให้ยาและความปลอดภัย
การศึกษาทางคลินิกโดยทั่วไปได้ใช้ นิโคตินาไมด์ในปริมาณสูงทางปาก (1.5–3.0 กรัม/วัน) ในการทดลองข้างต้น ผู้ป่วยได้รับยาเพิ่มขึ้นจาก 1500 เป็น 3000 มิลลิกรัมต่อวัน ปริมาณยาเหล่านี้สูงกว่าปริมาณที่รับประทานตามปกติมาก แต่ยังคงอยู่ในช่วงที่ทดสอบในการศึกษาด้านอื่นๆ (เช่น การวิจัยโรคอัลไซเมอร์) ข้อมูลเภสัชจลนศาสตร์แสดงให้เห็นว่า NAM ถูกเมตาบอไลซ์อย่างกว้างขวางในขั้นตอนแรก ดังนั้นมีเพียงส่วนน้อยเท่านั้นที่ไปถึงเนื้อเยื่อจอประสาทตา (pmc.ncbi.nlm.nih.gov). ดังนั้นปริมาณยาที่สูงจึงมีจุดประสงค์เพื่อเอาชนะข้อจำกัดนี้ ยังคงไม่ชัดเจนว่าปริมาณยาที่สูงกว่านี้จะมีประสิทธิภาพหรือทนทานได้ดีกว่าหรือไม่ การศึกษาในสัตว์มักใช้ปริมาณยาที่อิงตามน้ำหนักตัวที่สูงกว่ามาก ซึ่งทำให้เกิดข้อกังวลเกี่ยวกับความเป็นไปได้ในการใช้กับมนุษย์ (pmc.ncbi.nlm.nih.gov).
จนถึงตอนนี้ ความทนทานในระยะสั้นดูเหมือนจะดี การทดลองรายงานว่ามีเพียงอาการไม่สบายทางเดินอาหารเล็กน้อยเท่านั้นที่เป็นผลข้างเคียงที่พบบ่อยที่สุด ตัวอย่างเช่น บทความทบทวนฉบับหนึ่งพบว่าปริมาณยาไม่เกิน 3 กรัม/วัน เป็นเวลา 6–12 สัปดาห์ ได้รับการยอมรับได้ดี โดยไม่มีเหตุการณ์ไม่พึงประสงค์ร้ายแรงหรือการเพิ่มขึ้นของเอนไซม์ตับ (pmc.ncbi.nlm.nih.gov). ในการทดลองแบบครอสโอเวอร์ การปฏิบัติตามคำแนะนำเป็นไปอย่างดีเยี่ยม และ NAM “ได้รับการยอมรับได้ดีโดยมีผลข้างเคียงน้อยที่สุด” (www.researchgate.net). ในทำนองเดียวกัน การศึกษาของ JAMA ไม่พบปัญหาด้านความปลอดภัยร้ายแรงใดๆ บทความทบทวนของ IJMS ยืนยันว่าแม้แต่การรวม NAM+ไพรูเวท ก็ยังได้รับการยอมรับได้ดีในปริมาณสูง โดยมีเพียงอาการทางเดินอาหารเล็กน้อยและไม่มีเหตุการณ์ร้ายแรง (pmc.ncbi.nlm.nih.gov).
มีการรายงานการหยุดยาเพียงไม่กี่ราย ในการทดลองแบบเปิดขนาดเล็กของ NAM สำหรับโรคต้อหิน ผู้ป่วย 3 ใน 87 ราย (ประมาณ 3%) หยุดยาเนื่องจากผลข้างเคียง (ส่วนใหญ่เป็นทางเดินอาหาร) (pmc.ncbi.nlm.nih.gov). โดยรวมแล้ว ข้อมูลความปลอดภัยที่ดีของ NAM (ราคาถูก ใช้ทางปาก) เป็นสิ่งน่ายินดี (pmc.ncbi.nlm.nih.gov). อย่างไรก็ตาม ความปลอดภัยในระยะยาว ยังคงเป็นคำถามที่เปิดกว้าง การศึกษาส่วนใหญ่กินเวลาตั้งแต่ไม่กี่สัปดาห์ถึงสองสามเดือน นิโคตินาไมด์ไม่ใช่สารเฉื่อยโดยสมบูรณ์ – ในทางทฤษฎีแล้ว การใช้ยาในปริมาณที่สูงมากเป็นเวลาหลายปีอาจส่งผลต่อการทำงานของตับ สถานะเมทิลเลชัน หรือระบบอื่นๆ ได้ บทความทบทวนฉบับหนึ่งตั้งข้อสังเกตว่า แม้ NAM จะ “ได้รับการยอมรับได้ดีในระยะสั้น” แต่หลักฐานเกี่ยวกับการใช้ในระยะยาวนั้นมีจำกัด (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). การทดลองที่กำลังดำเนินอยู่จะติดตามเอนไซม์ตับและผลการตรวจทางห้องปฏิบัติการอื่นๆ เพื่อให้มั่นใจในความปลอดภัย การทดลอง NAM ที่ใหญ่ที่สุดในโลก (Nicotinamide Diabetes Intervention Trial) ใช้ยา 3 กรัม/วัน เป็นเวลา 3 ปี โดยไม่มีปัญหาสำคัญ แต่การนำไปใช้กับผู้ป่วยต้อหินยังคงต้องรอการศึกษา
การคัดเลือกผู้ป่วยและความหลากหลายของการตอบสนอง
ผู้ป่วยต้อหินทุกคนไม่คาดว่าจะตอบสนองได้เท่ากัน ข้อมูลที่มีอยู่ชี้ให้เห็นประโยชน์สูงสุดใน โรคระยะเริ่มต้นถึงปานกลาง ก่อนที่การสูญเสีย RNFL จะรุนแรงถึงขั้นสุดท้าย ในการทดลอง การปรับปรุงการมองเห็น/ERG พบได้ในส่วนที่มีความบกพร่องปานกลาง ในขณะที่ลานสายตาที่อยู่แล้วที่หรือต่ำกว่า “ค่าพื้นฐาน” ที่วัดได้นั้นไม่ได้รับการฟื้นฟูการทำงาน (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). สิ่งนี้บ่งชี้ว่าดวงตาที่มี RNFL บางมาก (ปรากฏการณ์ “ค่าพื้นฐาน” ในต้อหินระยะรุนแรง) อาจมีเซลล์ RGCs ที่มีชีวิตเหลือรอดน้อยเกินไปที่จะกู้คืนได้ ในทางตรงกันข้าม ผู้ป่วยที่มีการสูญเสียลานสายตาเล็กน้อยถึงปานกลางยังมีเซลล์ RGCs ที่ยังมีชีวิตอยู่แต่เครียดจำนวนมาก ซึ่งทำให้พวกเขาเป็นผู้สมัครที่เหมาะสมที่สุด
ตัวอย่างเช่น การศึกษา JAMA พบว่าจุดลานสายตาที่ดีขึ้นเมื่อได้รับ NAM/ไพรูเวท คือ “จุดที่มีการสูญเสียความไวเล็กน้อยถึงปานกลาง” ซึ่งสอดคล้องกับการช่วยฟื้นฟูเซลล์ที่ทำงานผิดปกติบางส่วน (pmc.ncbi.nlm.nih.gov). บทความทบทวนของ Biomedicines ยืนยันเช่นเดียวกัน โดยสังเกตว่าตำแหน่งที่มีความไวปานกลางมีการปรับปรุงมากที่สุด (pmc.ncbi.nlm.nih.gov). ในทางตรงกันข้าม ไม่มีผู้ป่วยรายใดแสดงการปรับปรุงโครงสร้าง (ความหนาของ RNFL) ในระยะสั้น ซึ่งชี้ให้เห็นว่า NAM ไม่ได้ช่วยให้แอกซอนงอกใหม่แต่เป็นการฟื้นฟูการทำงาน (pmc.ncbi.nlm.nih.gov). ดังนั้น ผู้ป่วยต้อหินระยะเริ่มต้นและมี RNFL เพียงพออาจได้รับประโยชน์สูงสุด
ปัจจัยอื่นๆ อาจส่งผลต่อการตอบสนองได้ ตัวอย่างเช่น โรคต้อหินมีความหลากหลาย (ความดันสูงเทียบกับความดันปกติ พื้นหลังทางพันธุกรรมที่แตกต่างกัน โรคร่วม) การทดลองหนึ่ง (Gustavsson 2023) ระบุว่าผู้ป่วยที่มีโรครุนแรงมีการเพิ่มขึ้นของการไหลเวียนเลือดในหลอดเลือดเมื่อได้รับ NAM ในปริมาณที่มากขึ้น (pmc.ncbi.nlm.nih.gov) ซึ่งบ่งชี้ว่าต้อหินรุนแรงอาจได้รับประโยชน์จากผลต่อหลอดเลือด แม้ว่าการตอบสนองของ RGC จะมีจำกัดก็ตาม อย่างไรก็ตาม การตรวจทางสรีรวิทยาไฟฟ้าและลานสายตาน่าจะดีขึ้นก็ต่อเมื่อมีเซลล์ RGCs เหลือรอดมากพอ สรุปคือ การคัดเลือกผู้ป่วยยังคงอยู่ระหว่างการศึกษา แต่สมมติฐานที่สมเหตุสมผลคือ ดวงตาที่อยู่ในระยะเริ่มต้นและมีภาวะเครียดทางเมตาบอลิซึม มีแนวโน้มที่จะได้รับการช่วยฟื้นฟูการทำงานมากที่สุด (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov).
การทดลองที่กำลังดำเนินอยู่
การทดลองขนาดใหญ่หลายโครงการกำลังดำเนินอยู่เพื่อประเมินการบำบัดด้วยนิโคตินาไมด์ในโรคต้อหินอย่างเข้มงวด:
- การทดลองระยะที่ 3 ของ University College London (NCT05405868) กำลังทดสอบ NAM ในปริมาณสูงถึง 3.0 กรัม/วัน ในการรักษาผู้ป่วยต้อหินมุมเปิดเป็นเวลา 27 เดือน (pmc.ncbi.nlm.nih.gov). ผลลัพธ์หลักคือการเปลี่ยนแปลงของความไวของลานสายตาเฉลี่ยเมื่อเวลาผ่านไป (pmc.ncbi.nlm.nih.gov).
- การทดลอง Umeå University Glaucoma Nicotinamide Trial (NCT05275738) วางแผนการให้ NAM 3.0 กรัม/วัน เป็นเวลา 2 ปี เทียบกับยาหลอก โดยเน้นที่อัตราการดำเนินของลานสายตา (pmc.ncbi.nlm.nih.gov).
- การทดลองที่นำโดยออสเตรเลีย (NCT04784234) กำลังประเมินอาหารเสริม “GlaucoCetin” (ซึ่งมี NAM และสารอื่นๆ) โดยมีจุดสิ้นสุดรวมถึงการตรวจทางสรีรวิทยาไฟฟ้าและความไวต่อความคมชัด (pmc.ncbi.nlm.nih.gov).
- Columbia University กำลังดำเนินการวิจัย RCT ของ NAM+ไพรูเวท (NCT05695027) เป็นเวลา 20 เดือน โดยมีผลลัพธ์รวมถึงลานสายตาส่วนกลางและความหนาของ OCT RNFL (pmc.ncbi.nlm.nih.gov).
การศึกษาเหล่านี้จะจัดการกับช่องว่างที่สำคัญ: ความคงทน ของผลกระทบ (ความก้าวหน้าตลอดหลายปี) ความสัมพันธ์เชิงโครงสร้าง (การเปลี่ยนแปลงของ OCT) และความเป็นไปได้ในโลกแห่งความเป็นจริง นอกจากนี้ยังจะมีการคัดเลือกกลุ่มผู้ป่วยที่มีขนาดใหญ่ขึ้นและมีความหลากหลายมากขึ้น ซึ่งอาจช่วยให้ทราบว่ากลุ่มย่อยใด (ความรุนแรง ชนิดของต้อหิน ระดับ NAD+ เริ่มต้น) ได้รับประโยชน์มากที่สุด
คำถามที่ยังไม่ได้รับคำตอบ
แม้จะมีข้อมูลเบื้องต้นที่น่าสนใจ แต่ก็ยังมีคำถามอีกมากมาย ยังไม่มีการสรุปว่า NAM เพียงแค่ให้ประโยชน์ด้านการทำงานในระยะสั้น หรือจริงๆ แล้ว ชะลอความเสื่อมของระบบประสาทในระยะยาว การปรับปรุงจะคงอยู่หรือไม่หลังจากหยุดการเสริม หรือจำเป็นต้องได้รับการรักษาอย่างต่อเนื่อง? ปริมาณและตารางเวลาที่เหมาะสม (เช่น ควรให้เป็นช่วงๆ หรือเป็นรอบ) ยังไม่เป็นที่ทราบแน่ชัด ปัจจัยเฉพาะของผู้ป่วย (เช่น เมตาบอลิซึมของ NAD+ ทั่วร่างกาย อาหาร พันธุกรรม) ที่คาดการณ์การตอบสนองยังไม่ได้ถูกระบุ และยังไม่ชัดเจนว่าการบำบัดด้วย NAM ควรจะบูรณาการเข้ากับกลยุทธ์การป้องกันระบบประสาทอื่นๆ ได้อย่างไร
ที่สำคัญคือ ผลลัพธ์เชิงโครงสร้างจนถึงขณะนี้ยังน่าผิดหวัง: ไม่มีการทดลองใดรายงานการเพิ่มขึ้นของความหนาของ RNFL หรือ ganglion cell complex สิ่งนี้ชี้ให้เห็นว่าการเติม NAD+ อาจช่วยยืดเวลาการทำงานได้ แต่ไม่สามารถทดแทนเซลล์ที่สูญเสียไปแล้วได้ การรักษาระยะยาวสามารถรักษาระดับความชันของ RNFL ได้หรือไม่เป็นคำถามสำคัญที่ยังเปิดกว้าง การวิจัยในอนาคตจะต้องติดตามดวงตาเป็นเวลาหลายปี
อย่างไรก็ตาม การทดลองที่มีอยู่ได้แสดงให้เห็นว่าการบำบัดเมตาบอลิซึมนั้น เป็นไปได้และปลอดภัย เพียงพอที่จะดำเนินการต่อไป ความหวังคือแนวทางที่มุ่งเป้าไปที่ NAD+ เหล่านี้จะเสริมการลด IOP แบบดั้งเดิม และในที่สุดจะกลายเป็นส่วนหนึ่งของการดูแลผู้ป่วยต้อหินแบบเฉพาะบุคคล
บทสรุป
นิโคตินาไมด์ในปริมาณสูงแสดงให้เห็นถึงความเป็นไปได้ทางชีวภาพและมีแนวโน้มที่ดีในการบำบัดทางคลินิกเบื้องต้นสำหรับการ “ช่วยฟื้นฟูเมตาบอลิซึม” ของ RGCs ในโรคต้อหิน การทดลองแบบสุ่มรายงานการปรับปรุงในระยะสั้นในการตรวจทางสรีรวิทยาไฟฟ้าและลานสายตา โดยเฉพาะอย่างยิ่งในบริเวณที่เสียหายเล็กน้อยถึงปานกลาง (www.researchgate.net) (pmc.ncbi.nlm.nih.gov). กลไกของนิโคตินาไมด์ – การเติม NAD+ เพื่อฟื้นฟูการทำงานของไมโทคอนเดรีย – เป็นเหตุผลที่น่าสนใจสำหรับการช่วยฟื้นฟูเซลล์ RGCs ที่ประสบภาวะเครียดก่อนที่เซลล์จะตาย (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). ข้อพิจารณาที่สำคัญรวมถึงการใช้ยาในปริมาณสูงถึงประมาณ 3 กรัม/วัน (ซึ่งได้รับการยอมรับได้ดีในช่วงหลายสัปดาห์) และการเฝ้าระวังผลข้างเคียงทางเดินอาหาร (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). เมื่อมีการเปิดเผยผลการทดลองแบบหลายศูนย์ขนาดใหญ่ขึ้นในอีกไม่กี่ปีข้างหน้า เราจะได้เรียนรู้ว่าการบำบัดเมตาบอลิซึมนี้สามารถชะลอการลุกลามของโรคต้อหินได้อย่างยั่งยืนหรือไม่ และผู้ป่วยกลุ่มใดมีแนวโน้มที่จะได้รับประโยชน์สูงสุด