บทนำ
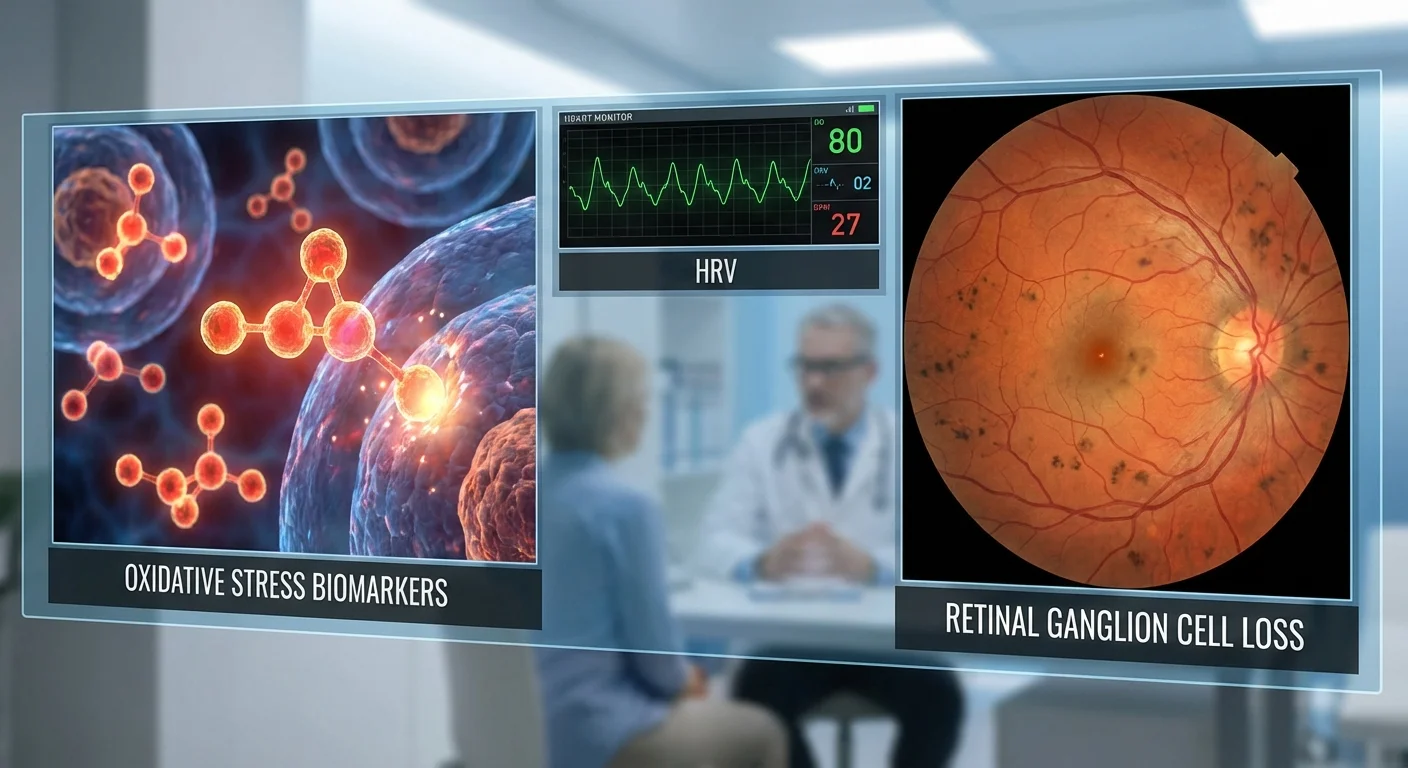
ต้อหินเป็นโรคตาที่ เซลล์เรตินากังเกลียน (RGCs) – ซึ่งเป็นเซลล์ประสาทที่ส่งสัญญาณภาพจากตาไปยังสมอง – ค่อย ๆ ตายลง สิ่งนี้ทำให้เกิดการสูญเสียการมองเห็นอย่างค่อยเป็นค่อยไปและไม่สามารถย้อนกลับได้ โดยปกติแล้วแพทย์จะเน้นไปที่การลดความดันตาเพื่อชะลอการลุกลามของต้อหิน แต่ปัจจุบันงานวิจัยแสดงให้เห็นว่า ความเครียดจากปฏิกิริยาออกซิเดชัน (oxidative stress) (ความเครียดทางเคมีชนิดหนึ่งในร่างกาย) และความไม่สมดุลของ ระบบประสาทอัตโนมัติ (autonomic nervous system) (ระบบประสาท “อัตโนมัติ” ที่ควบคุมสิ่งต่าง ๆ เช่น อัตราการเต้นของหัวใจ) ก็มีบทบาทเช่นกัน ในผู้ป่วยต้อหิน ระดับของ เครื่องบ่งชี้รีดอกซ์ (redox markers) บางชนิดในเลือด – ซึ่งเป็นสารที่บ่งบอกถึงความเสียหายจากปฏิกิริยาออกซิเดชัน – มักจะสูงกว่าปกติ ในขณะเดียวกัน ผู้ป่วยต้อหินจำนวนมากมี ความแปรปรวนของอัตราการเต้นของหัวใจ (HRV) ต่ำลง ซึ่งเป็นสัญญาณของความไม่สมดุลของระบบประสาทอัตโนมัติ การเพิ่มขึ้นของความเครียดจากปฏิกิริยาออกซิเดชันและการควบคุมระบบประสาทอัตโนมัติที่ไม่ดีอาจทำให้ RGCs เสียหายแย่ลง
ในบทความนี้ เราจะอธิบายว่าเครื่องบ่งชี้ความเครียดจากปฏิกิริยาออกซิเดชัน เช่น F2-ไอโซพรอสเทน (F2-isoprostanes), มาลอนไดอัลดีไฮด์ (MDA) และ 8-ไฮดรอกซี-2'-ดีออกซีควานโนซีน (8-OHdG) คืออะไร และพบได้อย่างไรในผู้ป่วยต้อหิน เราจะให้คำจำกัดความของ HRV (ความแปรปรวนของอัตราการเต้นของหัวใจ) และทบทวนว่ามีการเปลี่ยนแปลงอย่างไรในผู้ป่วยต้อหิน เราจะอธิบายเส้นทางชีวภาพที่เป็นไปได้ที่เชื่อมโยงความเครียดจากปฏิกิริยาออกซิเดชันและความไม่สมดุลของระบบประสาทอัตโนมัติกับการตายของ RGCs ที่เร็วขึ้น จากนั้นเราจะสรุปว่าการศึกษาเกี่ยวกับสารต้านอนุมูลอิสระ (สารอาหารที่ต่อสู้กับความเครียดจากปฏิกิริยาออกซิเดชัน) ได้แสดงผลลัพธ์อย่างไรต่อผู้ป่วยต้อหิน สุดท้าย เราจะเสนอการศึกษา “มัลติ-โอ้ห์มิกส์ (multi-omics)” ในอนาคตที่รวมเครื่องบ่งชี้รีดอกซ์ในเลือดหรือปัสสาวะ การวัด HRV และการถ่ายภาพจอตาขั้นสูง เพื่อข้อมูลเชิงลึกใหม่ ๆ
ตลอดบทความนี้ เราจะเน้นข้อมูลที่ผู้ป่วยสามารถเข้าใจและนำไปปฏิบัติได้ นอกจากนี้เราจะอธิบายว่าการทดสอบความเครียดจากปฏิกิริยาออกซิเดชันใดบ้างที่สามารถสั่งได้ (ผ่านทางเลือดหรือปัสสาวะ) และค่าที่สูงหรือต่ำอาจมีความหมายอย่างไรสำหรับผู้ที่กังวลเกี่ยวกับโรคต้อหิน
เครื่องบ่งชี้ความเครียดจากปฏิกิริยาออกซิเดชันในผู้ป่วยต้อหิน
ความเครียดจากปฏิกิริยาออกซิเดชัน (Oxidative stress) หมายถึงการมี “อนุมูลอิสระ” (โมเลกุลออกซิเจนที่ทำปฏิกิริยา) มากเกินไปในร่างกาย ทำให้เกิดความเสียหายต่อเซลล์ เราไม่สามารถวัดอนุมูลอิสระได้โดยตรงง่าย ๆ ดังนั้นแพทย์และนักวิจัยจึงใช้ ชีวภาพบ่งชี้ (biomarkers) ในเลือดหรือปัสสาวะที่บ่งบอกถึงความเสียหายจากปฏิกิริยาออกซิเดชัน เครื่องบ่งชี้ที่สำคัญสามอย่างในผู้ป่วยต้อหินคือ F2-ไอโซพรอสเทน (F2-isoprostanes), มาลอนไดอัลดีไฮด์ (MDA) และ 8-ไฮดรอกซี-2'-ดีออกซีควานโนซีน (8-OHdG) ทั้งสามชนิดนี้จะเพิ่มขึ้นเมื่อความเครียดจากปฏิกิริยาออกซิเดชันเพิ่มขึ้น
-
F2-ไอโซพรอสเทน (8-iso-PGF2α) – เป็นโมเลกุลที่เสถียรซึ่งเกิดขึ้นเมื่อไขมัน (ไขมันไม่อิ่มตัวหลายตำแหน่งในเยื่อหุ้มเซลล์) เกิดปฏิกิริยาออกซิเดชัน F2-ไอโซพรอสเทนถือเป็น “มาตรฐานทองคำ” สำหรับการวัดการออกซิเดชันของไขมัน (pmc.ncbi.nlm.nih.gov) ระดับที่สูงขึ้นในเลือดหรือปัสสาวะบ่งชี้ว่าเซลล์กำลังถูกโจมตีจากปฏิกิริยาออกซิเดชัน แม้ว่าจะไม่ใช่การศึกษาต้อหินทั้งหมดที่วัดค่าเหล่านี้ แต่พบระดับ F2-ไอโซพรอสเทนสูงในหลายโรคและเชื่อกันว่าสะท้อนถึงความเครียดจากปฏิกิริยาออกซิเดชันที่รุนแรง (pmc.ncbi.nlm.nih.gov) (ในทางปฏิบัติ ห้องปฏิบัติการสามารถวัด F2-ไอโซพรอสเทนในปัสสาวะหรือพลาสมาโดยใช้อุปกรณ์พิเศษ แต่ส่วนใหญ่จะทำในการตั้งค่าการวิจัย)
-
มาลอนไดอัลดีไฮด์ (MDA) – สารเคมีนี้ถูกผลิตขึ้นเมื่อโมเลกุลออกซิเจนที่ทำปฏิกิริยา (reactive oxygen species) สลายไขมันในร่างกาย เช่นเดียวกับ F2-ไอโซพรอสเทน มันบ่งบอกถึงความเสียหายของไขมันจากการออกซิเดชัน การศึกษาต้อหินหลายชิ้นพบว่าผู้ป่วยต้อหินมี MDA ในเลือดสูงกว่าคนปกติ (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) อันที่จริง การทบทวนขนาดใหญ่พบว่า MDA เป็นเครื่องบ่งชี้ความเครียดจากปฏิกิริยาออกซิเดชันที่สูงขึ้นอย่างสม่ำเสมอที่สุดในเลือดของผู้ป่วยต้อหิน (pmc.ncbi.nlm.nih.gov) ในการศึกษาผู้ป่วยต้อหินมุมปิด ผู้ป่วยมี MDA สูงกว่ากลุ่มควบคุมอย่างมีนัยสำคัญ (pmc.ncbi.nlm.nih.gov) โดยเฉพาะอย่างยิ่ง การศึกษานั้นแสดงให้เห็นว่าผู้ป่วยที่มีระดับ MDA สูงมาก มีการสูญเสียการมองเห็นที่เร็วขึ้น: ผู้ที่มี MDA สูงกว่าประมาณ 12 หน่วย มีการเสื่อมถอยของลานสายตาที่รวดเร็วขึ้นมาก (pmc.ncbi.nlm.nih.gov)
-
8-ไฮดรอกซี-2'-ดีออกซีควานโนซีน (8-OHdG) – เครื่องบ่งชี้นี้บ่งบอกถึงความเสียหายของ DNA (สารพันธุกรรมในเซลล์) จากปฏิกิริยาออกซิเดชัน เมื่อความเครียดจากปฏิกิริยาออกซิเดชันตัดหรือเปลี่ยน DNA ระดับ 8-OHdG จะเพิ่มขึ้นและสามารถวัดได้ในเลือดหรือปัสสาวะ การศึกษาผู้ป่วยต้อหิน (ในต้อหินความดันปกติและต้อหินลอกหลุด) พบว่าระดับ 8-OHdG ใน พลาสมา สูงกว่าในกลุ่มควบคุมอย่างมีนัยสำคัญ (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) ตัวอย่างเช่น การศึกษาหนึ่งพบว่า 8-OHdG ในเลือดเฉลี่ยประมาณ 17 ng/mL ในคนปกติ และประมาณ 23 ng/mL ในผู้ป่วยต้อหิน (pmc.ncbi.nlm.nih.gov) รายงานอื่นแสดงให้เห็นว่าความเสี่ยงต่อการเป็นต้อหินสูงกว่า 4 เท่าในผู้ที่มี 8-OHdG สูงกว่าค่าที่กำหนด (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) กล่าวโดยสรุปคือ 8-OHdG สูง หมายถึงความเสียหายของ DNA จากโมเลกุลออกซิเจนที่ทำปฏิกิริยามากขึ้น และสิ่งนี้พบได้ในผู้ป่วยต้อหิน
เครื่องบ่งชี้อื่น ๆ ที่บางครั้งมีการวัดรวมถึงระดับสารต้านอนุมูลอิสระทั้งหมด (เช่น “สถานะสารต้านอนุมูลอิสระรวม” หรือเอนไซม์เช่น superoxide dismutase (SOD) และ glutathione peroxidase) ในการศึกษาต้อหินหลายชิ้น สารต้านอนุมูลอิสระเหล่านี้มักจะต่ำ (เนื่องจากถูกใช้ไปกับการต่อสู้กับอนุมูลอิสระ) ในขณะที่เครื่องบ่งชี้เช่น MDA, 8-OHdG หรือ H₂O₂ สูง (pmc.ncbi.nlm.nih.gov) (เพื่อความกระชับ เราจะเน้นไปที่ F2-ไอโซพรอสเทน, MDA และ 8-OHdG ที่นี่ แต่หลายการศึกษารายงานเอนไซม์และวิตามินต้านอนุมูลอิสระที่ต่ำลงในผู้ป่วยต้อหิน)
สรุป: ในผู้ป่วยต้อหิน การศึกษาพบความเสียหายจากปฏิกิริยาออกซิเดชันในร่างกายที่สูงขึ้นอย่างสม่ำเสมอ เครื่องบ่งชี้เช่น MDA และ 8-OHdG มีแนวโน้มที่จะสูงกว่าช่วงปกติที่พบในคนปกติ (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) นักวิจัยเชื่อว่าความเครียดจากปฏิกิริยาออกซิเดชันที่มากเกินไปนี้มีส่วนทำให้เกิดผลกระทบของต้อหินต่อเส้นประสาทตา
การวัดความเครียดจากปฏิกิริยาออกซิเดชัน: การทดสอบที่มีอยู่
แม้ว่าเครื่องบ่งชี้เหล่านี้จะมีความสำคัญในการวิจัย แต่ก็ยังไม่เป็นการทดสอบทางคลินิกประจำ อย่างไรก็ตาม ห้องปฏิบัติการพิเศษและคลินิกสุขภาพบางแห่งมีการเสนอการตรวจวิเคราะห์ความเครียดจากปฏิกิริยาออกซิเดชัน นี่คือสิ่งที่ผู้ป่วยควรรู้:
-
การทดสอบ 8-OHdG: สามารถวัดได้ในพลาสมาในเลือดหรือในปัสสาวะ มีชุดตรวจเชิงพาณิชย์ (การทดสอบ ELISA) เพื่อวัด 8-OHdG ในปัสสาวะ (เช่น ชุดตรวจ Genox “8-OHdG Check” (www.genox.com)) ผู้ให้บริการด้านสุขภาพสามารถจัดให้มีการทดสอบนี้ผ่านห้องปฏิบัติการพิเศษ ไม่มีระดับ “ปกติ” สากล แต่การศึกษาให้แนวคิดบางอย่าง ตัวอย่างเช่น การศึกษาต้อหินหนึ่งพบว่าผู้ป่วยกลุ่มควบคุมมีค่าเฉลี่ยประมาณ 17 ng/mL ในขณะที่ผู้ป่วยต้อหินมีค่าเฉลี่ยประมาณ 23 ng/mL (pmc.ncbi.nlm.nih.gov) หากค่า 8-OHdG ของคุณสูงกว่าค่าปกติของคนสุขภาพดีมาก มันบ่งบอกถึงความเสียหายของ DNA ที่เพิ่มขึ้นจากความเครียดจากปฏิกิริยาออกซิเดชัน
-
การทดสอบ F2-ไอโซพรอสเทน: โดยปกติจะวัดจากตัวอย่างปัสสาวะ 24 ชั่วโมง หรือบางครั้งในเลือด ถือว่ามีความน่าเชื่อถือสูง แต่ต้องใช้อุปกรณ์ในห้องปฏิบัติการ (mass spectrometry) ค่าปกติขึ้นอยู่กับอายุและวิธีการ แต่ผลลัพธ์ที่สูงกว่ามากก็บ่งบอกถึงการเกิดออกซิเดชันของไขมันที่เพิ่มขึ้น การทดสอบนี้ส่วนใหญ่ทำในการวิจัยหรือศูนย์เชี่ยวชาญ
-
การทดสอบ MDA: มาลอนไดอัลดีไฮด์สามารถวัดได้ในพลาสมาในเลือด (มักใช้วิธี “thiobarbituric acid reactive substances” หรือ TBARS หรือโดยวิธีโครมาโทกราฟี) ช่วงค่าปกติของห้องปฏิบัติการแตกต่างกันไป แต่การศึกษาต้อหินหนึ่งใช้ค่า cutoff ประมาณ 12 µmol/L เพื่อบ่งชี้ความเสี่ยงที่สูงขึ้น (pmc.ncbi.nlm.nih.gov) หากรายงานผลจากห้องปฏิบัติการของคุณแสดงค่า MDA สูงกว่าค่าปกติ (สอบถามช่วงอ้างอิงของห้องปฏิบัติการ) นั่นอาจบ่งบอกถึงความเครียดจากปฏิกิริยาออกซิเดชันที่มากเกินไปต่อไขมัน
-
การทดสอบสารต้านอนุมูลอิสระรวมหรือเอนไซม์: ห้องปฏิบัติการบางแห่งวัด “ความสามารถในการต้านอนุมูลอิสระรวม” หรือระดับของ SOD หรือ glutathione peroxidase ผลลัพธ์ที่ต่ำกว่าปกติจะบ่งบอกถึงความเครียดจากปฏิกิริยาออกซิเดชันอีกครั้ง เนื่องจากสารต้านอนุมูลอิสระถูกใช้ไป
ในทางปฏิบัติ การทดสอบเหล่านี้ไม่เป็นมาตรฐานเหมือนการตรวจคอเลสเตอรอลหรือน้ำตาลในเลือด หากคุณต้องการตรวจ คุณอาจต้องขอให้ห้องปฏิบัติการเฉพาะทางหรือปรึกษาแพทย์ที่สามารถสั่งตรวจได้ โปรดทราบว่าผลลัพธ์ต้องได้รับการตีความในบริบทโดยผู้เชี่ยวชาญ ปัจจัยต่าง ๆ เช่น อาหาร ช่วงเวลาของวัน หรือการออกกำลังกายอาจส่งผลต่อเครื่องบ่งชี้เหล่านี้ได้
ตามที่การทบทวนหนึ่งชี้ให้เห็น ความเครียดจากปฏิกิริยาออกซิเดชัน ไม่ได้ถูกประเมินเป็นประจำในการปฏิบัติงานประจำวัน (pmc.ncbi.nlm.nih.gov) เนื่องจากโมเลกุลออกซิเจนที่ทำปฏิกิริยาเองมีอายุสั้น แทนที่จะเป็นเช่นนั้น แพทย์จะดูเครื่องบ่งชี้ทางอ้อม (ดังที่กล่าวมาข้างต้น) หรือเน้นไปที่การลดความเครียดผ่านวิถีชีวิต หากคุณได้รับผลการทดสอบ ให้เปรียบเทียบกับ “ช่วงปกติ” ที่ระบุ และปรึกษาแพทย์ของคุณ โดยทั่วไปแล้ว 8-OHdG, MDA หรือไอโซพรอสเทนที่ สูงกว่าปกติ บ่งบอกถึงความเครียดจากปฏิกิริยาออกซิเดชันที่เพิ่มขึ้น ในขณะที่ระดับที่อยู่ในช่วงปกติเป็นเรื่องที่น่าสบายใจ
การทำงานของระบบประสาทอัตโนมัติและความแปรปรวนของอัตราการเต้นของหัวใจในผู้ป่วยต้อหิน
ระบบประสาทอัตโนมัติ (ANS) ควบคุมการทำงานที่ไม่สมัครใจ เช่น อัตราการเต้นของหัวใจ, โทนัสของหลอดเลือด และการย่อยอาหาร มีสองสาขา – ซิมพาเทติก (มักเรียกว่า “สู้หรือหนี”) และพาราซิมพาเทติก (พักผ่อน/ย่อยอาหาร) ความสมดุลที่ดีระหว่างสองสาขาทำให้เกิดอัตราการเต้นของหัวใจที่แปรผันอยู่ตลอดเวลา ความแปรปรวนของอัตราการเต้นของหัวใจ (HRV) เป็นการวัดว่าเวลาที่ใช้ระหว่างการเต้นของหัวใจมีการผันผวนมากน้อยเพียงใด พูดง่าย ๆ คือ HRV ที่สูงขึ้นหมายความว่าหัวใจตอบสนองได้อย่างยืดหยุ่น (มักเป็นสัญญาณของสุขภาพที่ดี) ในขณะที่ HRV ที่ต่ำมากบ่งบอกถึง ความไม่สมดุลของระบบประสาทอัตโนมัติ ซึ่งมักเกิดจากกิจกรรมซิมพาเทติกที่มากเกินไป หรือโทนัสพาราซิมพาเทติกที่ลดลง
การศึกษาล่าสุดแสดงให้เห็นว่าผู้ป่วยต้อหินมักมี HRV ลดลง เมื่อเทียบกับคนที่ไม่เป็นต้อหิน (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) ตัวอย่างเช่น ในการศึกษาขนาดใหญ่หนึ่ง การศึกษาพบว่าผู้ป่วยที่มี ต้อหินลอกหลุด (ต้อหินมุมเปิดชนิดหนึ่ง) มีค่า HRV ต่ำกว่ากลุ่มควบคุมที่สุขภาพดีอย่างเห็นได้ชัด (pmc.ncbi.nlm.nih.gov) การวิเคราะห์อื่นพบว่าผู้ป่วยต้อหินที่มี HRV ต่ำที่สุด (การครอบงำของระบบประสาทซิมพาเทติกที่แข็งแกร่งที่สุด) มีการบางลงของชั้นเส้นประสาทตาในเรตินาที่เร็วกว่าผู้ที่มี HRV สูงกว่ามาก (pmc.ncbi.nlm.nih.gov) ในการศึกษานั้น กลุ่มที่มี HRV ต่ำสูญเสียความหนาของเส้นใยประสาทประมาณ 1.4 ไมโครเมตรต่อปี (เทียบกับเพียง 0.3 ไมโครเมตรต่อปีในกลุ่มที่มี HRV สูง) (pmc.ncbi.nlm.nih.gov) พวกเขายังมีความผันผวนของความดันตามากขึ้นและแรงดันการไหลเวียนโลหิตในลูกตาต่ำลง ซึ่งบ่งชี้ว่าความไม่สมดุลของระบบประสาทอัตโนมัติส่งผลต่อการไหลเวียนโลหิตในตา
กล่าวโดยสรุป ต้อหิน – โดยเฉพาะบางชนิด เช่น ต้อหินลอกหลุด – มักจะมาพร้อมกับการ ทำงานผิดปกติของ ANS การศึกษาพบอย่างสม่ำเสมอว่าผู้ป่วยต้อหินมีความผันแปรของอัตราการเต้นของหัวใจน้อยกว่าคนปกติ (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) HRV ที่ต่ำลงเป็นสัญญาณของความเครียดเรื้อรังหรือเส้นประสาทซิมพาเทติกที่ทำงานมากเกินไป ที่สำคัญคือ HRV ที่ต่ำในผู้ป่วยต้อหินมีความเชื่อมโยงกับผลลัพธ์ที่แย่ลง: ผู้ป่วยที่มี HRV ต่ำลง มีการสูญเสียเส้นใยประสาทตาที่เร็วกว่าและมีข้อบกพร่องของลานสายตาตรงกลางมากขึ้น (pmc.ncbi.nlm.nih.gov)
การวัด HRV: บุคคลสามารถวัด HRV ได้ด้วยอุปกรณ์เช่น เครื่องวัดอัตราการเต้นของหัวใจ หรือแม้กระทั่งสมาร์ทวอทช์และสมาร์ทโฟนบางรุ่นที่ใช้เซ็นเซอร์ชีพจร คลินิกบางครั้งใช้ ECG สั้น ๆ หรือเครื่องวิเคราะห์ HRV แบบพกพา (เช่น เซ็นเซอร์ปลายนิ้ว) หาก HRV ของคุณต่ำกว่าค่าเฉลี่ยสำหรับอายุและเพศของคุณ แสดงว่ามีความเครียดต่อระบบประสาทอัตโนมัติ ตัวอย่างเช่น การศึกษา [26] ใช้ SDNN (การวัด HRV มาตรฐาน) เพื่อแบ่งผู้ป่วยออกเป็นกลุ่ม HRV “ต่ำ” และ “สูง” แม้ว่าจะไม่มีค่า cutoff ง่าย ๆ ที่เผยแพร่สู่สาธารณะ แต่ SDNN ที่ต่ำกว่าประมาณ 50 ms มักถือว่าต่ำในผู้ใหญ่ อย่างไรก็ตาม ควรปรึกษาแพทย์ของคุณพร้อมข้อมูล HRV ดิบ พวกเขาอาจใช้ร่วมกับข้อมูลสุขภาพอื่น ๆ มากกว่าที่จะใช้เพียงอย่างเดียว
ความเชื่อมโยงกับความเครียดจากปฏิกิริยาออกซิเดชัน: HRV ที่ต่ำหมายความว่าร่างกายอยู่ในภาวะเครียดที่สูงขึ้น ในหลายสภาวะ (เช่น โรคไตเรื้อรังหรือโรคหัวใจ) นักวิจัยพบว่า เครื่องบ่งชี้ความเครียดจากปฏิกิริยาออกซิเดชันที่สูงขึ้นมักจะมาพร้อมกับ HRV ที่ต่ำลง (pmc.ncbi.nlm.nih.gov) ในการศึกษาผู้ป่วยโรคไตหนึ่ง การศึกษาพบว่าผู้ที่มีระดับ F2-ไอโซพรอสเทนในพลาสมาสูง (การวัดความเครียดจากปฏิกิริยาออกซิเดชัน) มี HRV ลดลงอย่างมีนัยสำคัญ (pmc.ncbi.nlm.nih.gov) แม้ว่าความเชื่อมโยงที่แน่ชัดนี้ยังไม่ได้มีการศึกษาอย่างกว้างขวางในผู้ป่วยต้อหิน แต่ก็บ่งบอกถึงวัฏจักร: ความเครียดจากปฏิกิริยาออกซิเดชันอาจส่งผลต่อหลอดเลือดและเส้นประสาท นำไปสู่ความไม่สมดุลของระบบประสาทอัตโนมัติ ซึ่งในทางกลับกันอาจทำให้การไหลเวียนโลหิตและความเครียดต่อดวงตาแย่ลง
ความเครียดจากปฏิกิริยาออกซิเดชันและความไม่สมดุลของระบบประสาทอัตโนมัติสามารถเร่งการสูญเสีย RGC ได้อย่างไร
เพื่อให้เข้าใจว่าความเครียดจากปฏิกิริยาออกซิเดชันและความไม่สมดุลของ ANS อาจ ทำให้เซลล์เรตินากังเกลียน (RGCs) ตายเร็วขึ้น ได้อย่างไร ให้พิจารณาเส้นทางที่เชื่อมโยงกันเหล่านี้:
-
ความเสียหายโดยตรงจากปฏิกิริยาออกซิเดชันต่อ RGCs: RGCs เป็นเซลล์ประสาทที่มีความต้องการพลังงานสูงมาก (โดยเฉพาะอย่างยิ่งแอกซอนที่ยาวและไม่มีเยื่อหุ้มไมอีลินในเรตินา) (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) พวกมันพึ่งพามิโตคอนเดรีย (โรงไฟฟ้าของเซลล์) อย่างมากในการผลิต ATP มิโตคอนเดรียตามธรรมชาติจะปล่อย โมเลกุลออกซิเจนที่ทำปฏิกิริยา (ROS) ออกมาในระหว่างการผลิตพลังงาน หากการผลิต ROS สูงเกินไป หรือการป้องกันสารต้านอนุมูลอิสระของเซลล์อ่อนแอ ROS ส่วนเกินจะสะสม ใน RGCs สิ่งนี้หมายถึงความเสียหายจากปฏิกิริยาออกซิเดชันต่อ DNA, โปรตีน และไขมัน ตัวอย่างเช่น 8-OHdG ถูกสร้างขึ้นเมื่อ ROS ทำลาย DNA ใน RGCs เมื่อ DNA และเยื่อหุ้มมิโตคอนเดรียเสียหาย กระบวนการสำคัญของเซลล์จะล้มเหลว ROS ที่สูงเรื้อรังจะกระตุ้นโปรแกรมการตายของเซลล์ในตัว (apoptosis) โดยการปล่อยปัจจัยเช่น cytochrome c จากมิโตคอนเดรีย (pmc.ncbi.nlm.nih.gov) พูดง่าย ๆ คือ ความเครียดจากปฏิกิริยาออกซิเดชันที่มากเกินไป วางยาพิษ RGCs และทำให้พวกมันทำลายตัวเอง สิ่งนี้พบได้ในการศึกษาดวงตาหลายชิ้น: พบ ROS ส่วนเกินในเซลล์จอตาหลังการบาดเจ็บ และการเพิ่มสารต้านอนุมูลอิสระสามารถยับยั้งความเสียหายในแบบจำลองสัตว์ได้ (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov)
-
ผลกระทบต่อหลอดเลือด (การไหลเวียนโลหิต): ความไม่สมดุลของระบบประสาทอัตโนมัติ (การทำงานเกินของระบบประสาทซิมพาเทติก) สามารถทำให้หลอดเลือดตีบแคบลงและลดการไหลเวียนโลหิตไปยังตา ในผู้ป่วยต้อหิน การมีเลือดไปเลี้ยงเพียงพอมีความสำคัญอย่างยิ่งต่อการอยู่รอดของ RGCs ตัวอย่างเช่น การศึกษา [26] แสดงให้เห็นว่าผู้ป่วยที่มี HRV ต่ำมี แรงดันการไหลเวียนโลหิตในลูกตา (ocular perfusion pressure) (แรงดันเลือดที่มีประสิทธิภาพที่ไปเลี้ยงเส้นประสาทตา) ต่ำกว่าและมีความผันผวนของความดันตาจากปีต่อปีมากขึ้น ความดันเลือดต่ำหรือความดันตาที่พุ่งสูงขึ้นอาจทำให้ RGCs ขาดออกซิเจนเป็นครั้งคราว ภาวะขาดเลือด (ischemia) เองก็ทำให้เกิดความเครียดจากปฏิกิริยาออกซิเดชัน – เมื่อได้รับออกซิเจนกลับคืนมา มันจะสร้าง ROS (การบาดเจ็บจากการขาดเลือดแล้วกลับคืนมา) ดังนั้น การหดตัวของหลอดเลือดที่ขับเคลื่อนโดย ANS และความไม่เสถียรของการไหลเวียนโลหิตจึงสร้างวัฏจักรของการขาดออกซิเจนและความเสียหายจากปฏิกิริยาออกซิเดชันต่อ RGCs (pmc.ncbi.nlm.nih.gov)
-
การอักเสบและความเครียดของเซลล์: ความเครียดจากปฏิกิริยาออกซิเดชันสามารถทำให้เซลล์ค้ำจุนในเรตินา (เซลล์เกลีย) อักเสบได้ จากนั้นเซลล์เหล่านี้จะปล่อยโมเลกุลที่ก่อให้เกิดการอักเสบซึ่งสร้างความเครียดเพิ่มเติมให้กับ RGCs ในขณะเดียวกัน การทำงานผิดปกติของระบบประสาทอัตโนมัติมักเชื่อมโยงกับการอักเสบระดับต่ำทั่วร่างกาย การรวมกันของ ROS ที่มากเกินไปและภาวะที่ถูกกระตุ้นโดยระบบประสาทซิมพาเทติกอาจเพิ่มการอักเสบที่เป็นอันตรายรอบ ๆ ส่วนหัวของเส้นประสาทตา ทำให้การตายของ RGCs เร็วขึ้น
-
ปฏิสัมพันธ์กับความเครียดทางกล: ความดันตาที่สูง (IOP) เองทำให้ส่วนหัวของเส้นประสาทตาผิดรูป ทำให้แอกซอนของ RGCs ยืดออก แอกซอนที่เครียดจะขาดพลังงานและผลิต ROS มากขึ้น หากสารต้านอนุมูลอิสระต่ำ (ดังที่พบในผู้ป่วยต้อหิน) ROS ส่วนเกินจะทำให้สมดุลเอียงไปสู่การตายของเซลล์ ความไม่สมดุลของ ANS อาจทำให้ความดันตาผันผวนแย่ลงและลดความสามารถของตาในการควบคุมความดันตาและการไหลเวียนโลหิต ทำให้ผลกระทบนี้เพิ่มขึ้น (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov)
โดยสรุป ความเครียดจากปฏิกิริยาออกซิเดชัน ทำลาย RGCs ในระดับเซลล์ ในขณะที่ ปัญหาเกี่ยวกับหลอดเลือดที่ควบคุมโดยระบบประสาทอัตโนมัติ ทำให้การไหลเวียนโลหิตและการรักษาของ RGCs บกพร่อง การทบทวนโรคต้อหินที่สำคัญได้สรุปไว้อย่างกระชับว่า การตายของเซลล์ RGCs แบบอะพอพโทซิสในผู้ป่วยต้อหินเกิดจาก IOP ที่สูงขึ้น การไหลเวียนโลหิตไม่ดี (“ภาวะหลอดเลือดไม่เพียงพอ”) และความเครียดจากปฏิกิริยาออกซิเดชัน (pmc.ncbi.nlm.nih.gov) ปัจจัยเหล่านี้ทำงานร่วมกัน: ความเครียดจากปฏิกิริยาออกซิเดชันทำลายมิโตคอนเดรียและ DNA ของ RGCs (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) ในขณะที่ความเครียดต่อระบบประสาทอัตโนมัติทำให้เกิดภาวะขาดเลือดในเรตินาและการขาดสารอาหาร นำไปสู่การตายของ RGCs แบบอะพอพโทซิสที่เร็วขึ้น ในผู้ป่วย สิ่งนี้แสดงออกเป็นการสูญเสียเส้นใยประสาทตาและการมองเห็นที่เร็วขึ้นเมื่อ HRV ต่ำ (pmc.ncbi.nlm.nih.gov) หรือเครื่องบ่งชี้ความเครียดจากปฏิกิริยาออกซิเดชันสูง (pmc.ncbi.nlm.nih.gov)
การบำบัดด้วยสารต้านอนุมูลอิสระและผลลัพธ์ของต้อหิน
เนื่องจากต้อหินเกี่ยวข้องกับความเสียหายจากปฏิกิริยาออกซิเดชัน การศึกษาหลายชิ้นจึงตั้งคำถามว่า อาหารเสริมสารต้านอนุมูลอิสระ สามารถช่วยปกป้องดวงตาได้หรือไม่ สารต้านอนุมูลอิสระรวมถึงวิตามิน (C, E) สารอาหารเช่น โคเอนไซม์คิวเทน, ฟลาโวนอยด์ (ในผลไม้/ชา), กรดไขมันโอเมก้า 3 และสารสกัดจากพืช (เช่น ใบแปะก๊วย) สารเหล่านี้สามารถต่อต้านอนุมูลอิสระได้ อย่างน้อยก็ในทางทฤษฎี
ผลการวิจัยในห้องปฏิบัติการและสัตว์: ในแบบจำลองสัตว์ที่เป็นต้อหินหรือได้รับบาดเจ็บที่ตา การให้สารต้านอนุมูลอิสระมักจะช่วยลดการสูญเสีย RGCs ตัวอย่างเช่น ในหนูที่มีต้อหินหรือภาวะขาดเลือดในเรตินา อาหารเสริมเช่น วิตามินเอ, ใบแปะก๊วย, กรดอัลฟาไลโปอิก, โคเอนไซม์คิวเทน, กรดไขมันโอเมก้า 3 และเรสเวอราทรอล ล้วนแสดงการปกป้องเซลล์จอตาบางส่วน (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) ตารางการทบทวนหนึ่งรายการแสดงการทดลองจำนวนมาก: เช่น สารสกัดจากใบแปะก๊วยลดการตายของ RGCs ในดวงตาหนูที่มีความดันสูง (pmc.ncbi.nlm.nih.gov); โคเอนไซม์คิวเทนและวิตามินอีปกป้องเซลล์จอตาที่เพาะเลี้ยงจากสารพิษที่ก่อให้เกิดปฏิกิริยาออกซิเดชัน (pmc.ncbi.nlm.nih.gov); และสารต้านอนุมูลอิสระจากอาหาร (เช่น แอนโทไซยานินจากผลไม้) ช่วยรักษาสภาพโครงสร้างจอตาในแบบจำลองสัตว์ที่เป็นต้อหิน (pmc.ncbi.nlm.nih.gov) การศึกษาเหล่านี้ชี้ให้เห็นว่าสารต้านอนุมูลอิสระสามารถช่วยให้เซลล์จอตาอยู่รอดจากความเครียดได้
การทดลองทางคลินิกในมนุษย์: การทดลองในผู้ป่วยต้อหินมีขนาดเล็กกว่าและให้ผลลัพธ์ที่หลากหลาย แต่บางส่วนก็น่าสนับสนุน การทบทวนอย่างเป็นระบบล่าสุดของการทดลองแบบสุ่ม 15 ชิ้นพบว่าอาหารเสริมสารต้านอนุมูลอิสระ ช่วยปรับปรุงผลลัพธ์ที่เกี่ยวข้องกับต้อหินได้อย่างมีนัยสำคัญ (pmc.ncbi.nlm.nih.gov) โดยเฉลี่ย ผู้ป่วยที่รับประทานสารต้านอนุมูลอิสระ (วิตามิน, โคเอนไซม์คิวเทน, ลูทีน ฯลฯ) มีความดันตาต่ำลง การสูญเสียลานสายตาช้าลง และการไหลเวียนโลหิตในลูกตาดีขึ้นกว่าผู้ที่ได้รับยาหลอก (pmc.ncbi.nlm.nih.gov) ที่สำคัญคือไม่มีผลข้างเคียงเพิ่มเติม (เช่น การเปลี่ยนแปลงความดันโลหิต) ในกลุ่มที่ได้รับสารต้านอนุมูลอิสระเมื่อเทียบกับยาหลอก ดังนั้นจึงดูเหมือนปลอดภัย (pmc.ncbi.nlm.nih.gov)
ผลการวิจัยในมนุษย์ที่เฉพาะเจาะจงบางประการ: ในการทดลองปี 2003 ผู้ป่วยต้อหินที่รับประทานสารสกัดจากใบแปะก๊วยมีการปรับปรุงเล็กน้อยในดัชนีลานสายตา (pmc.ncbi.nlm.nih.gov) การศึกษาในภายหลังยืนยันว่าผู้ป่วย NVG (ต้อหินความดันปกติ) ที่รับประทานใบแปะก๊วยมีการไหลเวียนโลหิตรอบเส้นประสาทตาดีขึ้น (pmc.ncbi.nlm.nih.gov) การทดลองขนาดเล็กอื่น ๆ พบประโยชน์สำหรับสารสกัดจากชาเขียว (epigallocatechin gallate) ต่อการทำงานของเรตินา หรือแอนโทไซยานินจากแบล็คเคอร์แรนต์ที่ช่วยเพิ่มการไหลเวียนโลหิตในลูกตา (แม้ว่า IOP หรือการมองเห็นจะไม่เปลี่ยนแปลงมากนัก) (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) การรวมกันของสารสกัดจากพืช (ฟอร์สโคลิน+รูติน) ยังช่วยลด IOP ได้ประมาณ 10% นอกเหนือจากยาหยอดตาปกติ (pmc.ncbi.nlm.nih.gov)
อย่างไรก็ตาม ต้องยอมรับว่าผลลัพธ์มีความแปรปรวน การทดลองสารต้านอนุมูลอิสระบางส่วนแสดงผลลัพธ์ที่ดีขึ้นเล็กน้อยหรือไม่พบการเปลี่ยนแปลงเลย ความแตกต่างในปริมาณยา ชนิดของผู้ป่วย และขนาดของการศึกษามีความสำคัญ โดยรวมแล้ว หลักฐานส่วนใหญ่ชี้ให้เห็นว่าการเพิ่มสารต้านอนุมูลอิสระเป็น แนวโน้มที่ดีและปลอดภัย แต่ยังไม่ใช่การรักษาเด็ดขาด การทบทวนที่สำคัญสรุปว่าสิ่งเหล่านี้ อาจ ช่วยชะลอความเสียหายจากต้อหินได้ (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) แต่ยังคงต้องการการศึกษาที่ใหญ่ขึ้นและชัดเจนกว่านี้
ข้อคิดที่นำไปปฏิบัติได้: อย่างน้อยที่สุด การรับประทานอาหารที่มีประโยชน์ซึ่งอุดมไปด้วยสารต้านอนุมูลอิสระ (ผลไม้, ผักใบเขียว, โอเมก้า 3) ดูเหมือนจะเป็นสิ่งที่ดีต่อสุขภาพตา จักษุแพทย์บางท่านแนะนำอาหารเสริมเช่น วิตามิน C/E, ลูทีน หรือโอเมก้า 3 ให้กับผู้ป่วยต้อหินเป็นมาตรการเสริม ตรวจสอบกับแพทย์ของคุณก่อนเริ่มรับประทานยาเม็ดใด ๆ โดยเฉพาะในปริมาณที่สูง งานวิจัยจนถึงขณะนี้ชี้ให้เห็นว่าอาหารเสริมดังกล่าว จะไม่เป็นอันตรายและอาจช่วย ในบางแง่มุมของต้อหิน เช่น การไหลเวียนโลหิตหรือสุขภาพของเส้นประสาท (pmc.ncbi.nlm.nih.gov)
ทิศทางในอนาคต: การบูรณาการรีดอกซ์, HRV และการถ่ายภาพจอตา
ปัจจุบันนักวิจัยจินตนาการถึง การศึกษาแบบบูรณาการ มากขึ้น – ที่เรียกว่า มัลติ-โอ้ห์มิกส์ (multi-omics) – เพื่อเอาชนะโรคต้อหิน ซึ่งหมายถึงการรวบรวมข้อมูลหลายประเภทเข้าด้วยกัน: เครื่องบ่งชี้ในเลือด (หรือปัสสาวะ) ของความสมดุลรีดอกซ์, การบันทึก HRV อย่างต่อเนื่อง, ภาพจอตาที่ละเอียด และแม้แต่ข้อมูลทางพันธุกรรมหรือเมแทบอลิซึม ด้วยการนำชิ้นส่วนทั้งหมดมารวมกัน เราอาจพบรูปแบบที่มองไม่เห็นเมื่อพิจารณาแยกส่วน
ตัวอย่างเช่น เมแทบอโลมิกส์สมัยใหม่ (การวัดโมเลกุลขนาดเล็กหลายสิบชนิดในเลือด) ได้เผยให้เห็นลักษณะเฉพาะในผู้ป่วยต้อหินแล้ว การทบทวนการศึกษาเมแทบอโลมิกส์ในมนุษย์พบว่าระดับกรดอะมิโน, ไขมัน และเส้นทางที่เกี่ยวข้องมีการเปลี่ยนแปลงในผู้ป่วยต้อหิน (pmc.ncbi.nlm.nih.gov) การเปลี่ยนแปลงทางเมแทบอลิซึมเหล่านี้บ่งบอกถึงกระบวนการพื้นฐานที่สามารถกำหนดเป้าหมายได้ การรวมข้อมูลนั้นเข้ากับข้อมูล HRV (ปฏิสัมพันธ์ระหว่างลำไส้-สมอง-ANS) และการถ่ายภาพ OCT ความละเอียดสูงของเส้นประสาทตาและชั้นจอตา นักวิจัยสามารถจัดกลุ่มผู้ป่วยออกเป็นกลุ่มย่อยได้ บางทีผู้ป่วยบางรายอาจมีลักษณะเฉพาะแบบ “ความเครียดจากปฏิกิริยาออกซิเดชันสูง” (8-OHdG สูงมาก, HRV ต่ำ และชั้นเส้นใยประสาทตาบางลงเมื่อตรวจด้วย OCT) ในขณะที่บางรายไม่มี
สามารถมองเห็นคู่ขนานได้ในการวิจัยเกี่ยวกับภาวะเบาหวานขึ้นจอตา: การศึกษาล่าสุดในหนูได้ใช้วิธีการแบบมัลติ-โอ้ห์มิกส์ โดยรวมทรานสคริปโทมิกส์ของเนื้อเยื่อเรตินา, เมแทบอโลมิกส์ของซีรัมในเลือด และข้อมูลทางพันธุกรรม (GWAS) เพื่อเชื่อมโยงการเปลี่ยนแปลงเมแทบอไลต์ในเลือดกับการอักเสบของเรตินาในระยะแรก (pmc.ncbi.nlm.nih.gov) การประยุกต์ใช้กลยุทธ์ที่คล้ายกันกับต้อหิน – เช่น การเชื่อมโยงเมแทบอลิซึมส่วนปลายกับการสูญเสียเส้นใยประสาทตา – อาจนำไปสู่การค้นพบเป้าหมายยาใหม่หรือเครื่องหมายคัดกรอง ตัวอย่างเช่น หากเมแทบอไลต์ในเลือดบางชนิดเพิ่มขึ้นอย่างสม่ำเสมอ ก่อน การสูญเสียการมองเห็นใด ๆ พวกมันอาจกลายเป็นชีวภาพบ่งชี้เตือนล่วงหน้าได้
สิ่งนี้หมายความว่าอย่างไรสำหรับผู้ป่วย: ในอนาคต การมาพบแพทย์อาจเกี่ยวข้องกับการตรวจเลือด (หรือปัสสาวะ) แบบชุดสำหรับเครื่องบ่งชี้ความเครียดจากปฏิกิริยาออกซิเดชันหลายชนิด การวัด HRV (เช่น การตรวจ ECG ห้านาที หรือเครื่องวัดแบบสวมใส่ที่บ้าน) และการถ่ายภาพดวงตาขั้นสูง การวิเคราะห์ผลลัพธ์ทั้งหมดเข้าด้วยกันสามารถทำนายได้ว่าใครมีความเสี่ยงสูงสุดต่อการดำเนินโรค ยิ่งไปกว่านั้น หากพบว่าชีวภาพบ่งชี้เฉพาะ (เช่น F2-ไอโซพรอสเทนที่สูงมาก) เป็นตัวขับเคลื่อนความเสียหาย เราอาจปรับแต่งการรักษาเพื่อลดความเครียดนั้น หรือใช้สารต้านอนุมูลอิสระที่มุ่งเป้าเฉพาะเจาะจง
สำหรับตอนนี้ เรายังไปไม่ถึงจุดนั้น แต่การวิจัยต้อหินแบบมัลติ-โอ้ห์มิกส์เป็นทิศทางที่มีแนวโน้มที่ดี ความหวังคือการก้าวข้ามการเน้นที่ความดันตาเพียงอย่างเดียว และสร้างภาพรวมของโรคของผู้ป่วยแต่ละรายที่สมบูรณ์ยิ่งขึ้น
สรุป
ต้อหินเป็นมากกว่าแค่ความดันตาที่สูง – มันเชื่อมโยงกับความเครียดจากปฏิกิริยาออกซิเดชันที่แพร่หลายในร่างกายและการทำงานผิดปกติของระบบประสาทอัตโนมัติ ผู้ป่วยต้อหินมักมีระดับเครื่องบ่งชี้ในเลือดเช่น MDA และ 8-OHdG สูงขึ้น ซึ่งบ่งบอกถึงความเสียหายของเซลล์และ DNA (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) ในขณะเดียวกัน พวกเขามักแสดง ความแปรปรวนของอัตราการเต้นของหัวใจที่ต่ำลง ซึ่งสะท้อนถึงการทำงานเกินของระบบประสาทซิมพาเทติก (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) ปัจจัยทั้งสองนี้น่าจะทำงานร่วมกันเพื่อฆ่าเซลล์เรตินากังเกลียนได้เร็วขึ้น ความเครียดจากปฏิกิริยาออกซิเดชันทำลายมิโตคอนเดรียและ DNA ของ RGCs (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) ในขณะที่ความไม่สมดุลของระบบประสาทอัตโนมัตินำไปสู่การไหลเวียนโลหิตในตาที่ไม่ดีและความดันตาที่ผันผวน (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov)
มีหลักฐานที่ดีว่าสารต้านอนุมูลอิสระสามารถช่วยได้ – การศึกษาในสัตว์แสดงการปกป้อง RGCs อย่างสม่ำเสมอ (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) และการทดลองในมนุษย์บ่งชี้ว่าอาหารเสริมสามารถปรับปรุงลานสายตาและการไหลเวียนโลหิตในตาได้ (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov) ผู้ป่วยสามารถปรึกษาเรื่องวิตามินและสารอาหารต้านอนุมูลอิสระกับจักษุแพทย์ได้ ซึ่งเป็นส่วนหนึ่งของแนวทางวิถีชีวิตสุขภาพดี
ที่สำคัญคือ การทดสอบความเครียดจากปฏิกิริยาออกซิเดชันบางอย่าง (8-OHdG, MDA, ไอโซพรอสเทนในเลือดหรือปัสสาวะ) สามารถเข้าถึงได้ แม้ว่าจะไม่ใช่การตรวจประจำ หากมีการวัดค่าเหล่านี้ ค่าที่สูงขึ้น (เช่น 8-OHdG สูงกว่าประมาณ 20 ng/mL มาก หรือ MDA สูงกว่าช่วงค่าที่ห้องปฏิบัติการกำหนด) ควรแจ้งให้ใส่ใจกับอาหาร, วิถีชีวิต และอาจพิจารณาการสนับสนุนด้วยสารต้านอนุมูลอิสระ ในทำนองเดียวกัน การวัด HRV (ด้วยเครื่องวัดง่าย ๆ ที่บ้านหรือ ECG ที่คลินิก) สามารถบ่งบอกถึงสุขภาพของระบบประสาทอัตโนมัติได้ HRV ที่ต่ำอาจหมายถึงความเครียดเพิ่มเติมต่อดวงตา
ในอนาคต การรวมมาตรการเหล่านี้เข้ากับการถ่ายภาพจอตาขั้นสูงและข้อมูลทางพันธุกรรมในการศึกษาแบบบูรณาการอาจนำไปสู่ยุคใหม่ของการดูแลต้อหินแบบเฉพาะบุคคล สำหรับตอนนี้ การรับทราบข้อมูลเกี่ยวกับความเครียดจากปฏิกิริยาออกซิเดชันและสุขภาพหัวใจในผู้ป่วยต้อหินเป็นสิ่งสำคัญ การได้รับสารอาหารที่ดี การลดความเครียด และการตรวจสุขภาพเป็นประจำยังคงเป็นกุญแจสำคัญในการปกป้องการมองเห็นของคุณ