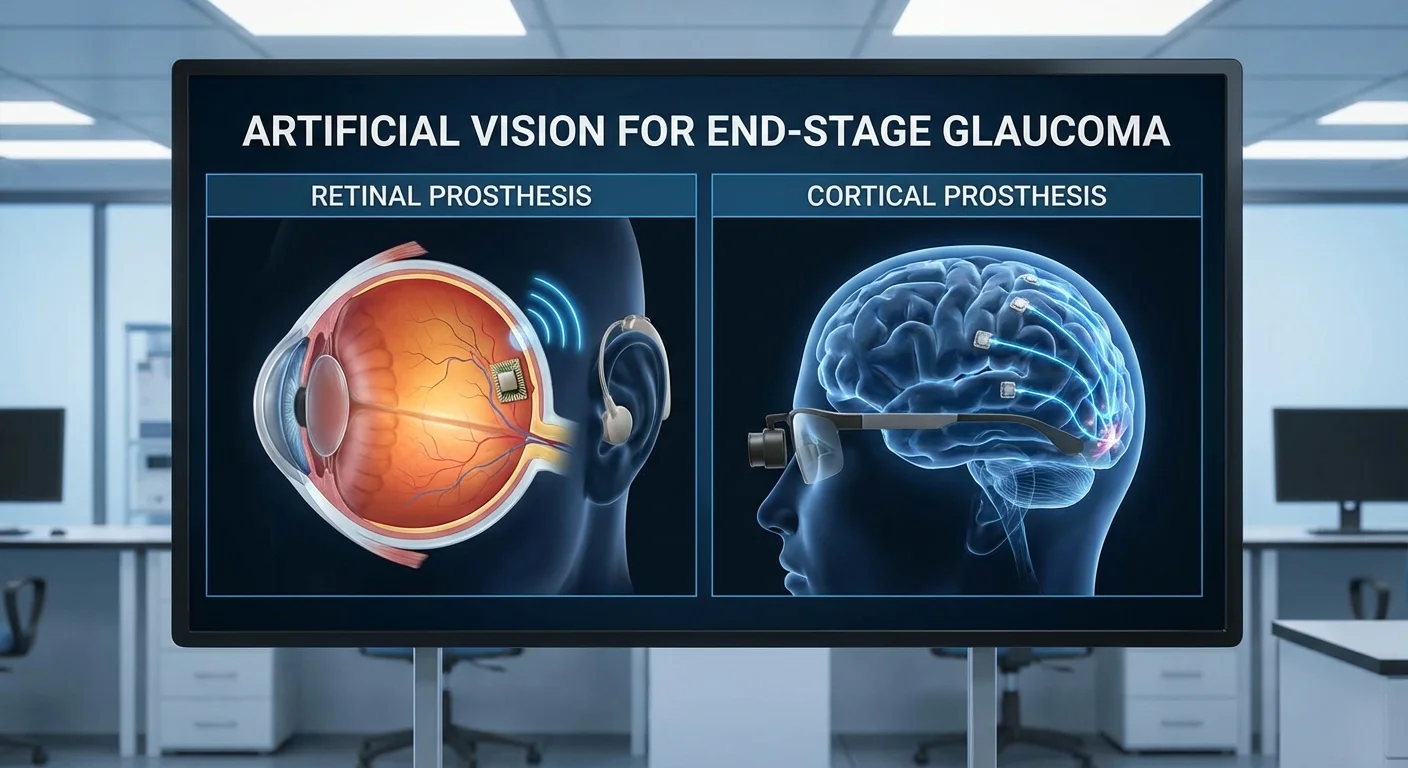
Visión Artificial para el Glaucoma Terminal: Prótesis Retinianas vs. Corticales
El glaucoma avanzado destruye el nervio óptico y las células ganglionares de la retina (CGR), dejando a los pacientes ciegos. La visión artificial (prótesis visual) busca sortear este daño. La mayoría de las prótesis existentes se dirigen a la retina o al nervio óptico, pero en el glaucoma terminal esas vías están destruidas. En su lugar, los investigadores están explorando implantes que estimulan directamente la corteza visual (cerebro). Este artículo compara las prótesis intrarretinianas (basadas en el ojo) frente a las corticales (basadas en el cerebro) para la ceguera por glaucoma.
En condiciones como la retinitis pigmentosa o la degeneración macular, los fotorreceptores mueren, pero las CGR y el nervio óptico permanecen intactos (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Los implantes retinianos funcionan en estos casos. Por ejemplo, Argus II (un implante epirretiniano) recibió la aprobación de la FDA para la retinitis pigmentosa en 2013 (pmc.ncbi.nlm.nih.gov). Estos dispositivos pueden restaurar la percepción básica de la luz y la detección de movimiento (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Sin embargo, el glaucoma es diferente: las CGR y el nervio óptico están destruidos, por lo que una señal de un implante retiniano no tiene a dónde ir (pubmed.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). En pruebas novedosas como el ensayo inicial de ORION, el objetivo es "sortear por completo la anatomía ocular enferma" enviando señales eléctricas directamente a la corteza visual del cerebro (pmc.ncbi.nlm.nih.gov).
En resumen, los implantes retinianos requieren neuronas retinianas supervivientes y un nervio óptico intacto (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Están diseñados para enfermedades de la retina externa (pérdida de fotorreceptores) donde las CGR aún existen (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Por el contrario, los implantes corticales están destinados a pacientes con degeneración retiniana interna grave o daño del nervio óptico (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Para el glaucoma avanzado (sin CGR), los enfoques corticales son la única opción protésica realista (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov).
Implantes Intrarretinianos
Las prótesis intrarretinianas (a menudo llamadas "ojos biónicos") utilizan una cámara externa (generalmente en gafas) para capturar imágenes y convertirlas en pulsos eléctricos. Estos pulsos se administran a través de una matriz de microelectrodos colocada sobre o debajo de la retina (pmc.ncbi.nlm.nih.gov). Los implantes epirretinianos (como Argus II) se colocan en la superficie retiniana adyacente a las CGR, mientras que los implantes subretinianos se sitúan debajo de la retina entre los fotorreceptores. También existen diseños supracoroideos (electrodos entre la retina y la esclera). En todos los casos, el objetivo es estimular eléctricamente las neuronas retinianas restantes.
Requisitos y Candidatos
Los candidatos para implantes retinianos deben haber perdido la visión fotorreceptora, pero aún conservar una retina interna intacta (células ganglionares y bipolares) (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Los candidatos típicos son aquellos con retinitis pigmentosa en fase terminal o atrofia geográfica (degeneración macular avanzada), no pacientes con glaucoma. Los pacientes con glaucoma carecen de CGR viables, por lo que las prótesis retinianas generalmente no pueden funcionar para ellos (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov).
Procedimiento Quirúrgico y Riesgos
La implantación de un dispositivo retiniano requiere un cirujano vitreorretiniano. Son necesarios procedimientos como una vitrectomía pars plana (extracción del gel vítreo) y la colocación de la matriz de electrodos (www.sciencedirect.com). En comparación con la cirugía cerebral, la cirugía retiniana es menos compleja. Los implantes epirretinianos son “menos complicados y [conllevan] menores niveles de riesgo durante la implantación” que los dispositivos corticales (pmc.ncbi.nlm.nih.gov). Sin embargo, pueden ocurrir complicaciones graves relacionadas con el ojo. En un ensayo de Argus II con 30 pacientes, por ejemplo, la mitad de los participantes experimentaron eventos adversos relacionados con el dispositivo o la cirugía durante 5 años (pmc.ncbi.nlm.nih.gov). Los problemas más comunes fueron la erosión conjuntival (ojo rojo) y la hipotonía ocular (presión ocular anormalmente baja) (pmc.ncbi.nlm.nih.gov). En general, aproximadamente el 40% de los sujetos tuvieron un evento adverso grave (la mitad de los cuales fueron reversibles) (pmc.ncbi.nlm.nih.gov). Las revisiones sistemáticas confirman que los implantes epirretinianos tienden a tener más complicaciones que los diseños subretinianos o supracoroideos (pmc.ncbi.nlm.nih.gov).
Resolución Espacial y Rendimiento Visual
Los implantes retinianos actuales producen una visión de muy baja resolución. Por ejemplo, la matriz de 6x10 de Argus II (60 electrodos) es análoga a una cámara de 6x10 píxeles. En la práctica, la mayoría de los sujetos solo pueden percibir patrones muy básicos de luz y oscuridad. Los estudios informan que los usuarios de implantes epirretinianos pueden localizar formas de alto contraste y detectar el movimiento mejor con el dispositivo encendido (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). En una revisión sistemática, el rendimiento en una tarea de "localización de cuadrados" de alto contraste mejoró hasta en un 89% con el implante activo (pmc.ncbi.nlm.nih.gov). Aun así, la agudeza visual con estos dispositivos sigue siendo extremadamente deficiente; incluso los mejores casos registrados fueron solo alrededor de 20/460 a 20/550 en términos de Snellen (pmc.ncbi.nlm.nih.gov) (muy por debajo del umbral de 20/200 para la ceguera legal).
Los implantes subretinianos (como el sistema Alpha IMS/AMS) han logrado una densidad ligeramente mayor (cientos de píxeles fotodiodos en lugar de decenas de electrodos). Un resumen reciente informó agudezas de rejilla de hasta 3,33 ciclos por grado (equivalente a aproximadamente 20/460 de visión) y cierta capacidad para reconocer movimientos simples y letras grandes (pmc.ncbi.nlm.nih.gov). Sin embargo, incluso estos representan solo una visión rudimentaria.
Entrenamiento y Adaptación
Los usuarios de implantes retinianos requieren un entrenamiento y rehabilitación extensos para interpretar las señales visuales inusuales. Los pacientes de ensayos clínicos suelen someterse a meses de entrenamiento con terapeutas visuales. Por ejemplo, los participantes del ensayo Argus II fueron “seleccionados meticulosamente” y se les proporcionó un entrenamiento exhaustivo sobre el uso del dispositivo (pmc.ncbi.nlm.nih.gov). Aprendieron tareas como localizar un cuadrado brillante, detectar el movimiento y reconocer formas básicas. Sin embargo, este entorno de laboratorio tan favorable puede no reflejar el uso en el mundo real; un estudio encontró que los usuarios comerciales a menudo confían menos en el implante en el día a día, debido a problemas de usabilidad (pmc.ncbi.nlm.nih.gov).
Resultados Funcionales y Calidad de Vida
Incluso con miles de dólares en tecnología, la visión restaurada es muy limitada. Los objetivos realistas para los implantes retinianos incluyen la navegación y orientación y la localización gruesa de objetos, en lugar de la lectura o el reconocimiento facial. En los ensayos del Argus II, los pacientes tuvieron un rendimiento notablemente mejor en tareas de orientación y movilidad con el implante activado (pmc.ncbi.nlm.nih.gov). Muchos podían detectar puertas o ventanas, seguir líneas brillantes en el suelo y localizar objetos grandes. En la vida diaria, los usuarios informan mejoras en la movilidad y la independencia. Una revisión sistemática encontró que los receptores de implantes retinianos informaron una mejor orientación y movilidad, lo que les ayudó con las tareas diarias (pmc.ncbi.nlm.nih.gov). Sin embargo, la visión sigue estando lejos de ser normal: los autores del estudio advierten que, incluso con el dispositivo, la agudeza se mantuvo por debajo de 20/200 (ceguera legal) (pmc.ncbi.nlm.nih.gov).
Implantes Corticales
Las prótesis visuales corticales adoptan un enfoque muy diferente: eluden el ojo y estimulan directamente el cerebro. Los electrodos se colocan sobre o dentro de la corteza visual (la región cerebral en la parte posterior de la cabeza que procesa la vista). Una cámara externa y un procesador convierten las imágenes en patrones de estimulación eléctrica que se envían de forma inalámbrica a estos electrodos corticales. Dado que la señal omite la retina y el nervio óptico, este método funciona incluso cuando esas estructuras están destruidas.
Cómo Funcionan
Por ejemplo, el sistema ORION de Second Sight utiliza una rejilla de electrodos colocada en la corteza occipital (creando fosfenos —puntos de luz— en el campo visual del paciente) (pmc.ncbi.nlm.nih.gov). Otro diseño (el ICVP de Illinois) utiliza matrices de electrodos penetrantes en la corteza (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). En un ensayo, se implantó una matriz Utah de 96 electrodos en la corteza visual de un voluntario ciego. La estimulación eléctrica allí produjo puntos de luz azul-blanca intermitentes que seguían el campo visual. Impresionantemente, el paciente pudo distinguir los bordes de los objetos e incluso identificar diferentes letras por sus contornos (pmc.ncbi.nlm.nih.gov). Estos resultados iniciales muestran que un implante cortical puede de hecho crear visión con patrones en un cerebro humano.
Criterios para Candidatos
Los implantes corticales están destinados a personas con ceguera completa e intratable y sin visión útil. En la práctica, los protocolos de los ensayos requieren ninguna percepción de la luz en ninguno de los ojos (www.ninds.nih.gov) (pmc.ncbi.nlm.nih.gov). Por ejemplo, un ensayo clínico de Orion acepta pacientes con ceguera bilateral (percepción luminosa mínima o peor) debido a daño en cualquier parte de la vía visual (enfermedad retiniana, lesión del nervio óptico, glaucoma, etc.) (www.ninds.nih.gov). Cualquier resto de visión haría que alguien no fuera elegible, ya que la cirugía cerebral invasiva podría poner en riesgo esa visión residual (pmc.ncbi.nlm.nih.gov). De hecho, los estudios enfatizan que las personas elegibles para implantes retinianos (aquellas con retina interna intacta) generalmente son malos candidatos para implantes corticales (pmc.ncbi.nlm.nih.gov). Así, los dispositivos corticales representan la opción final para la restauración de la visión en individuos totalmente ciegos.
Riesgos Quirúrgicos
Las prótesis corticales requieren neurocirugía (craneotomía) para implantar electrodos en el cerebro. Esto es, obviamente, más invasivo que la cirugía ocular. Los riesgos potenciales incluyen accidente cerebrovascular, infección o daño neurológico. En la práctica, pequeños ensayos de viabilidad han demostrado seguridad quirúrgica hasta ahora, pero los tamaños de muestra son minúsculos. Por ejemplo, un ensayo inicial de ORION implantó su matriz de 60 electrodos en seis sujetos ciegos sin eventos adversos graves relacionados con el implante (pmc.ncbi.nlm.nih.gov). (Los seis informaron ver fosfenos con el dispositivo encendido). Sin embargo, los expertos advierten que la cirugía cerebral debe abordarse con mucha cautela, razón por la cual solo se consideran candidatos completamente ciegos (pmc.ncbi.nlm.nih.gov).
Resolución Espacial y Rendimiento Visual
La resolución espacial de los implantes corticales también es muy baja en la actualidad. Los dispositivos existentes tienen como máximo unas pocas decenas de electrodos. ORION, por ejemplo, utilizó 60 electrodos en la corteza (pmc.ncbi.nlm.nih.gov). Incluso con docenas de electrodos, la "imagen" que percibe un paciente es extremadamente granulada. En el ensayo mencionado con 96 electrodos, los pacientes solo pudieron percibir patrones muy simples (líneas, letras sencillas). Lograr un detalle más fino requeriría cientos o miles de electrodos distribuidos en múltiples parches de la corteza, una tecnología que aún no existe para los humanos.
El entrenamiento es igualmente intensivo. Al igual que con los sistemas retinianos, los pacientes corticales deben aprender a interpretar su entrada visual anormal. Los informes iniciales sugieren que los pacientes pueden aprender a reconocer formas y letras grandes con el tiempo, pero esto justifica una rehabilitación prolongada. Todavía no hay datos publicados sobre regímenes de entrenamiento formales para implantes corticales, pero por analogía con los ensayos retinianos, esperamos que se necesitarían años de entrenamiento especializado para alcanzar cualquier utilidad práctica.
Resultados Funcionales
Ninguna prótesis cortical ha producido aún un nivel de visión cercano a lo normal. Hasta ahora, los objetivos son conservadores: navegación y localización de objetos. Los ensayos se centran en tareas como identificar objetos grandes y brillantes, detectar el movimiento y evitar obstáculos. Como señaló una revisión, las prótesis visuales pueden ser de gran ayuda en la orientación y la navegación, tareas en las que las tecnologías actuales para ciegos (como las aplicaciones para teléfonos inteligentes) aún se quedan cortas (pmc.ncbi.nlm.nih.gov). En entornos experimentales, animales ciegos con prótesis de estimulación cerebral han navegado con éxito laberintos utilizando señales artificiales. En ensayos en humanos, el único paciente que identificó letras mediante ORION solo reconoció caracteres muy grandes y aislados (pmc.ncbi.nlm.nih.gov).
En resumen, los primeros estudios de implantes corticales muestran que los pacientes pueden percibir patrones de luz simples y usarlos para adivinar formas o letras. Esto sugiere posibles beneficios para tareas como localizar puertas o encontrar bordes. Sin embargo, el reconocimiento fino de objetos (por ejemplo, caras o texto) está muy lejos de las capacidades actuales. Aún no se han informado mediciones de calidad de vida para implantes corticales; los ensayos en curso planean incluir resultados informados por los pacientes y pruebas funcionales (www.ninds.nih.gov) para ver si se producen mejoras en la vida diaria.
Resumen Comparativo
-
Complejidad quirúrgica: Los implantes retinianos implican cirugía ocular (vitrectomía y colocación de electrodos retinianos). Los implantes corticales requieren cirugía cerebral (craneotomía y matriz de electrodos corticales). La cirugía epirretiniana es bastante rutinaria para los especialistas en retina, mientras que la implantación cortical conlleva un riesgo neurológico inherentemente mayor. Una revisión reciente señala que incluso una visión residual leve se perdería si se operara el cerebro (pmc.ncbi.nlm.nih.gov), lo que subraya el riesgo de la cirugía cortical.
-
Resolución espacial: Ambos enfoques ofrecen actualmente una visión de muy baja resolución. Los dispositivos retinianos utilizan del orden de 60-150 electrodos o píxeles, produciendo solo patrones de luz rudimentarios (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Las matrices corticales también oscilan entre decenas y pocos cientos. Ninguno de los enfoques puede producir más que formas muy toscas. La agudeza visual reportada en dispositivos retinianos rara vez supera los ~20/500 (pmc.ncbi.nlm.nih.gov). La agudeza cortical es aún más difícil de definir, pero se espera que sea igualmente baja dado el pequeño número de electrodos.
-
Entrenamiento/adaptación: Todos los pacientes implantados necesitan una rehabilitación extensa. Los participantes en ensayos clínicos reciben un entrenamiento intensivo y guiado para aprender cómo los fosfenos corresponden a su entorno (pmc.ncbi.nlm.nih.gov). Esto es cierto tanto para los implantes retinianos como para los corticales. En la práctica, muchos usuarios encuentran el entrenamiento constante una carga, lo que puede limitar la frecuencia con la que realmente usan el dispositivo (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov).
-
Calidad de vida: Los implantes retinianos han demostrado algunos beneficios modestos en la calidad de vida. Los usuarios a menudo informan de una mejor orientación, una navegación más fácil en espacios familiares y ayuda con tareas diarias que dependen de la detección de luz versus oscuridad o formas grandes (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Ningún implante cortical ha demostrado aún una mejora clara en la calidad de vida, pero los investigadores están incorporando medidas de calidad de vida y función diaria en los ensayos en curso (pmc.ncbi.nlm.nih.gov) (www.ninds.nih.gov).
-
Resultados realistas: Ninguno de los enfoques restaurará la visión normal. Los pacientes solo deben esperar sensaciones visuales muy básicas. Los objetivos prácticos incluyen detectar puertas o ventanas, diferenciar habitaciones claras de oscuras, localizar obstáculos grandes o reconocer letras o formas muy grandes. La navegación (caminar por una habitación sin chocar con objetos) es un caso de uso realista a corto plazo (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). La lectura o el reconocimiento facial siguen estando más allá de las capacidades actuales.
-
Selección de candidatos: En la práctica, los pacientes que aún son candidatos potenciales para implantes retinianos (que tienen parte de la retina interna intacta) no serán derivados a ensayos corticales (pmc.ncbi.nlm.nih.gov). Por el contrario, los ensayos corticales requieren pacientes con ceguera total (sin visión residual) por cualquier causa (incluido el glaucoma) (www.ninds.nih.gov) (pmc.ncbi.nlm.nih.gov). Por ahora, un candidato típico para implante cortical es alguien que no puede beneficiarse en absoluto de los dispositivos retinianos (por ejemplo, capa de CGR destruida o nervio óptico seccionado).
Cronología y Estatus Regulatorio
El desarrollo de prótesis retinianas comenzó hace más de 20 años. El Argus II (Second Sight) es un hito: la aprobación de la FDA llegó en 2013 (pmc.ncbi.nlm.nih.gov) (después de una marca CE anterior en Europa). Argus II siguió siendo el único sistema aprobado comercialmente en todo el mundo hasta que la empresa detuvo la producción en 2019 (pmc.ncbi.nlm.nih.gov). Aproximadamente al mismo tiempo, algunos dispositivos subretinianos obtuvieron la aprobación CE en Europa, por ejemplo, los sistemas Alpha IMS (2013) y AMS (2016) (pmc.ncbi.nlm.nih.gov), pero ninguno está aprobado por la FDA. Muchos dispositivos retinianos ahora están descontinuados o en transición, con solo unos pocos (como PRIMA de Pixium y el implante supracoroideo de Bionic Vision) en ensayos actuales (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov).
Las prótesis corticales se encuentran en una etapa mucho más temprana. El primer implante cortical humano (Brindley-Dobelle en la década de 1970) fue puramente experimental. Hoy en día, Second Sight (ahora llamada Cortigent/Vivani) ha liderado un nuevo esfuerzo: su sistema ORION comenzó un ensayo de viabilidad temprana en 2017 (www.cortigent.com), y a partir de 2022 se fusionaron en Vivani Medical trabajando en una actualización ORION II (pmc.ncbi.nlm.nih.gov). Ningún dispositivo cortical ha obtenido aún aprobación regulatoria. Los estudios actuales (como el de Orion y el estudio ICVP de Illinois (pmc.ncbi.nlm.nih.gov)) se enumeran como ensayos de viabilidad temprana (p. ej., NCT03344848), con el objetivo de evaluar la seguridad y la función básica.
Hitos clave hasta la fecha: Ensayos de Argus II (retina) 2007–2009, aprobación de la FDA 2013, descontinuación 2019 (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Alpha IMS subretinal CE 2013, AMS mejorado CE 2016 (pmc.ncbi.nlm.nih.gov). Los primeros ensayos de Orion (cortical) comenzaron ~2017, con estudios de seguimiento en curso (aún sin aprobaciones) (pmc.ncbi.nlm.nih.gov). Próximos: Ensayos de Fase I de otros sistemas corticales (CORTIVIS en España, ICVP en EE. UU.) están reclutando participantes (pmc.ncbi.nlm.nih.gov) (www.ninds.nih.gov). Durante la próxima década, los desarrolladores esperan aumentar el número de electrodos y la interfaz cerebral para mejorar los resultados, pero por ahora tanto las prótesis retinianas como las corticales siguen siendo altamente experimentales.
Conclusión
Para la mayoría de los pacientes con glaucoma con daño terminal del nervio óptico, los implantes retinianos no son una opción porque la vía neural está seccionada. Las prótesis visuales corticales, por lo tanto, representan la única estrategia viable de visión artificial. Los estudios iniciales muestran que los dispositivos corticales pueden provocar patrones de luz simples incluso cuando el ojo está ciego (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Sin embargo, tanto los enfoques retinianos como los corticales ofrecen actualmente solo una visión rudimentaria. Los implantes retinianos tienen una historia clínica ligeramente más larga (algunas aprobaciones de la FDA/CE en otras enfermedades) y mejoras demostrables, aunque limitadas, en la movilidad y la orientación (pmc.ncbi.nlm.nih.gov) (pmc.ncbi.nlm.nih.gov). Los implantes corticales están en la etapa de viabilidad: evitan el nervio óptico, pero deben superar los desafíos de la cirugía cerebral, el mapeo de señales y el entrenamiento del paciente. Los objetivos realistas para cualquiera de los enfoques son la navegación básica y la localización de objetos, no la visión de alto detalle. Plazos: los dispositivos retinianos han estado en ensayos durante 15-20 años (con algunos productos comerciales que surgieron y luego desaparecieron) (pmc.ncbi.nlm.nih.gov), mientras que los sistemas corticales apenas están comenzando las pruebas en humanos. La autorización regulatoria en EE. UU./UE para implantes corticales aún está a años de distancia.
En resumen, para el glaucoma severo sin nervio óptico, los implantes corticales ofrecen esperanza. Pero los pacientes y los médicos deben comprender las limitaciones actuales: incluso los dispositivos de "visión biónica" más avanzados restauran solo la percepción de encendido/apagado de la luz y formas simples. La investigación en curso tiene como objetivo aumentar el número de electrodos, mejorar la biocompatibilidad y refinar el procesamiento de señales, pero en la actualidad la visión funcional de cualquier prótesis será extremadamente básica. Los pacientes deben tener expectativas realistas (por ejemplo, distinguir una puerta de una pared, no leer texto) y estar preparados para una rehabilitación extensa. Los futuros hitos a observar incluyen la finalización de los ensayos en curso de implantes corticales y cualquier aprobación de dispositivos de próxima generación.